ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 27.11.2019
Просмотров: 4045
Скачиваний: 98
NO-
СИНТАЗНАЯ СИГНАЛЬНАЯ СИСТЕМА
Роль N0 в качестве одной из важнейших сигнальных мо-
лекул в растениях была установлена сравнительно недавно,
хотя к этому времени NO-сигнальной системе животных и ее
роли в воспалительных процессах, апоптозе клеток и выра-
ботке иммунитета к патогенам было посвящено очень много
работ, и это привело к тому, что в 1992 г. NO была признана
редакцией журнала "Science" "молекулой года". N0 образу-
ется из аргинина, НАДФН и кислорода в результате реакции,
катализируемой ферментом NO-синтазой [Меньшикова и
др., 2000; Wendehenne et al., 2001] - стартовым ферментом
NO-
синтазной сигнальной системы (рис. 29):
2Аргинин + ЗНАДФН + 4О
2
+ ЗН
+
-> ->
2Цитруллин + 2NO + ЗНАДФ
+
+ 4Н
2
О.
NO-
синтаза принадлежит к числу наиболее сложных
ферментов, причем активность проявляет гомодимерная
форма фермента, а каждый неактивный мономер состоит
из редуктазного (НАДФН-ФАД-ФМН) и оксигеназного
(Fe-
гем) доменов, между которыми распологается кальмо-
дулин. Электроны, участвующие в окислении азота гуани-
динового радикала аргинина и образовании NO, транспор-
тируются из редуктазного в оксигеназный домен (рис. 30).
Имеется несколько изоформ фермента: мембраносвязан-
ные кальцийзависимые конститутивные, а также раствори-
мые кальцийнезависимые индуктивные (цитозольные), вы-
полняющие роль первого фермента NO-сигнальной цепи.
Недавно появилась информация о возможности местонахож-
дения NO-синтаз в пероксисомах клеток растений [Corpas et
al., 2001].
До сих пор неясно, какая из этих изоформ играет глав-
ную сигнальную роль. Нет данных об участии G-белков в
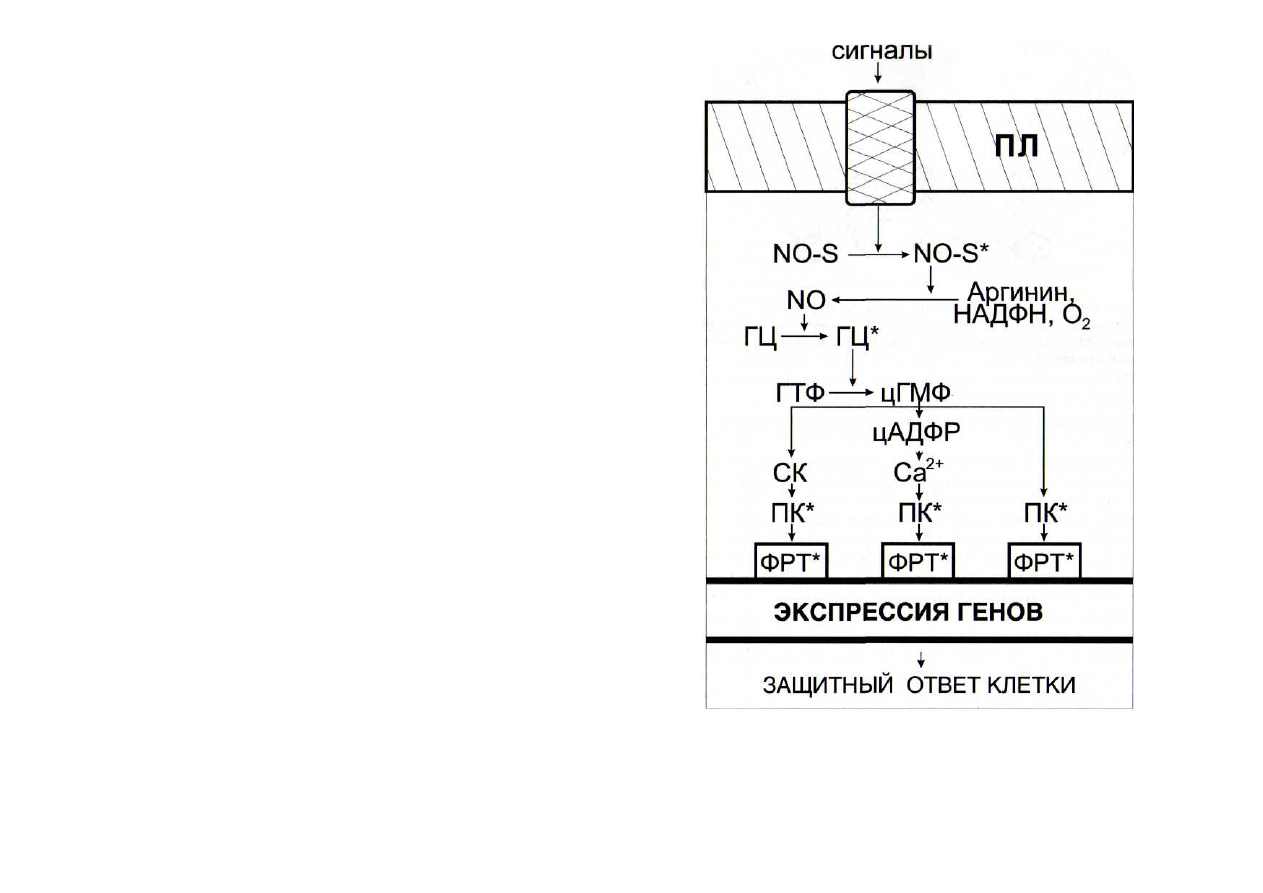
Рис. 29. Схема функционирования NO-синтазной сигнальной сис-
темы
ГЦ - гуанилатциклаза; СК - салициловая кислота; цАДФР - цикли-
ческая АДФ-рибоза; NO-S - NO-синтаза. Остальные обозначения - см.
рис. 6
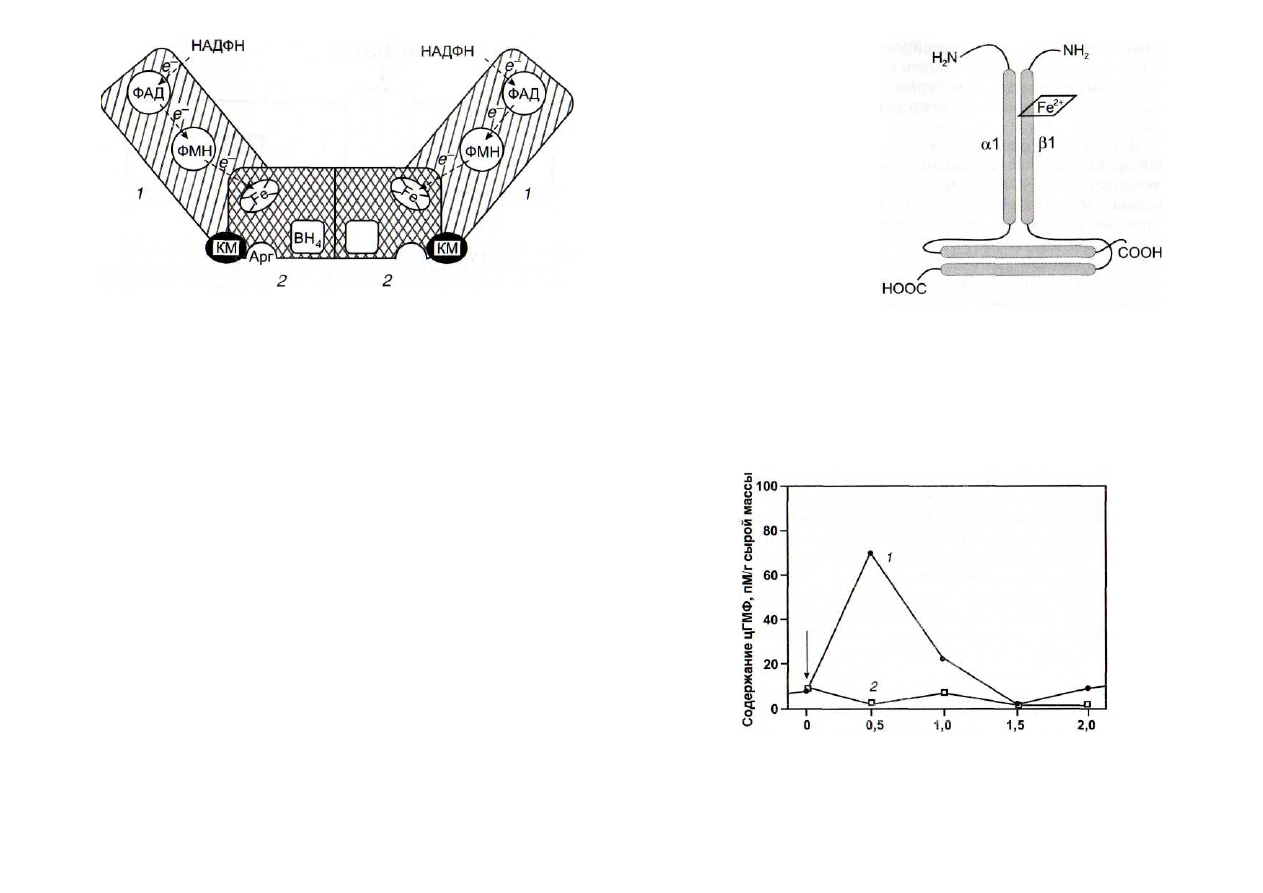
Рис. 30. Структура NO-синтазы [Горрен, Майер, 1998]
/ -
редуктазный домен; 2 - оксигеназный домен; Apr - остаток ар-
гинина; КМ - кальмодулин; ФАД и ФМН - флавиновые нуклеотиды;
ВН
4
-
птеридин; Fe - гем
передаче элиситорного сигнала от рецепторов к NO-син-
тазам.
NO-
синтаза у растений была обнаружена практически
одновременно в нескольких лабораториях [Cueto et al., 1996;
Leshem, 1996; Ninnemann, Maier, 1996; Noritake et al., 1996].
Для нас особый интерес представляют исследования, в ко-
торых была показана роль N0 в абиотических и биотиче-
ских стрессах [Leshem, Haramathy, 1996; Haramathy, Leshem,
1997; Huang, Knopp,
1998]. Оказалось, что активация NO-
синтазы происходит у устойчивых к патогенам растений
[Delledone et al., 1998; Klessig et al.,
2000], а образующийся
NO
вызывает синтез фитоалексинов и защитных белков
[Noritake et al., 1996; Dangl, 1998; Delledone et al.,
1998]. Выз-
ванное патогенами и элиситорами многократное повыше-
ние содержания NO в тканях растений стали называть "NO-
взрывом", по аналогии с "окислительным взрывом"
[Foissneretal., 2000].
С 1998 г. начинается интенсивный поиск сходства и
различий в функционировании NO-сигнальных систем у
животных и растений. Было найдено, что, так же как у
животных, в качестве сигнальных посредников между NO
и геномом выступают цГМФ- и цАДФ-рибоза (см. рис. 29)
Рис. 31. Структура диме-
ра цитоплазматической
гуанилатциклазы,
со-
стоящей из al- и (31-
субъединиц [Denninger,
Marietta, 1999] Fe
2+
-
гем
[Delledone et al., 1998;
Durner et al., 1998;
Hausladen,
Stamler,
1998], что раститель-
ная NO-синтаза инги-
бируется теми же со-
единениями, что и
животная.
цГМФ образуется из ГТФ с помощью растворимой цито-
плазматической гетеродимерной гуанилатциклазы. Одна из
субъединиц фермента содержит гем, связанный с остатком
гистидина (рис. 31). Активация гуанилатциклазы происхо-
дит при взаимодействии NO с гемом [Denninger, Marietta,
1999]. Необходимо отметить, что NO-индуцируемое накоп-
Бремя воздействия NO, ч
Рис. 32. Влияние NO на образование цГМФ в суспензии клеток
табака [Durner et al., 1998]
I
-
клетки, обработанные донором NO;
2 -
контроль. Стрелкой по-
казано начало воздействия NO
ление цГМФ имеет преходящий характер (рис. 32). Участие
цГМФ в сигнальной сети клеток определяется его способ-
ностью активировать некоторые протеинкиназы, откры-
вать катионные каналы и регулировать активность фосфо-
диэстераз.
В отличие от животных, в NO-синтазной системе расте-
ний принимает участие салициловая кислота в качестве по-
средника между N0 и геномом [Durner et al., 1998; Hausladen,
Stamler, 1998; McDowell, Dangl, 2000; Kumar, Klessig, 2000].
Изучение с помощью иммуноблотинга синтеза некоторых
белков, индуцируемых различными интермедиатами NO-
синтазной системы, в сочетании с использованием ингиби-
торов гуанилатциклазы и трансгенных растений с привне-
сенным бактериальным геном салицилат-гидроксилазы по-
зволил прийти к выводу о разветвленной структуре этого
сигнального пути. О первой точке ветвления можно судить
по открытию цГМФ-зависимой и независимой NO-индук-
ции фенилаланин-аммиак-лиазы, о второй - по NO-индуци-
рованному салицилатзависимому образованию матричных
РНК белка PR-1 и NO-индуцированному салицилатнезави-
симому образованию фенилаланин-аммик-лиазы [Durner et
al.,
1998]. Многократное накопление салицилата под влия-
нием NO было показано во многих работах, и в связи с этим
были оправданы исследования взаимосвязей NO и салици-
лата при функционировании NO-синтазной сигнальной сис-
темы. Существование NO-индуцированного цАДФрибоза-
зависимого- и цАДФрибозанезависимого синтеза белков
(PR-1) [Klessig et al.,
2000] предполагает еще одну точку
ветвления NO-сигнального пути. Обслуживает NO-синтаз-
ную систему, помимо NO-синтазы, еще целый ряд фермен-
тов, активируемых различными интермедиатами этого сиг-
нального пути [Klessig et al., 2000]. Монооксид азота активи-
рует гуанилатциклазу, катализирующую образование
цГМФ, который, в свою очередь, активирует цГМФ-зависи-
мую протеинкиназу, а последняя - факторы регуляции
транскрипции (NO -> цГМФ -> ПК -> ФРТ -> геном) и каль-
циевые каналы (NO —> цГМФ —» активация кальциевых ка-
налов —> повышение концентрации ионов кальция в цитозо-
ле —> Са-зависимые ПК —> ФРТ -> геном). Салициловая кис-
лота, накапливающаяся в результате гидролиза глюкозил-
салицилата или активации ФАЛ, способна активировать
специальную изоформу МАР-киназы (СК —> салицилатин-
дуцируемая МАР-киназа -» ФРТ -> геном). Циклический
гуанозинмонофосфат способен активировать АДФ-рибо-
зил-циклазу, катализирующую образование цАДФрибозы,
а последняя открывает кальциевые каналы (цГМФ —»
цАДФрибоза —> повышение содержания Са
2+
в цитозоле -»
Са-зависимые ПК —> ФРТ —> геном).
NO
является весьма активным свободным радикалом
(время его жизни in vivo составляет, по-видимому, немно-
гим более 10 с), он способен взаимодействовать с нуклеи-
новыми кислотами и белками неферментативно (рис. 33).
Так, было обнаружено, что у животных NO изменяет ак-
тивность железорегуляторного белка цитоплазмы (ЖРБ),
который связывает специфический элемент матричных
РНК и поэтому активирует или ингибирует их [Klausner et
al.,
1997]. Оказалось, что у растений NO оказывал влияние
на изоформу ЖРБ - аконитазу, вызывая ее ингибирова-
ние, что косвенно свидетельствует (наряду с существова-
нием протяженных консервативных последовательностей
у этих ферментов) о возможности влияния NO на процес-
сы трансляции непосредственно, неферментативно, минуя
классические и относительно долгие ферментативные сиг-
нальные пути. По-видимому, NO может влиять и на про-
цессы транскрипции, если учитывать факт ингибирования
им ДНК-связывающей активности факторов регуляции
транскрипции при S-нитрозилировании определенного ци-
стеинового остатка. Кроме того, обнаружено, что экзоген-
ный NO активировал ДНК-метилтрансферазу, что приво-
дило к повышению содержания метилированных остатков
цитозина в ДНК и, вследствие этого, препятствовало свя-
зыванию факторов регуляции транскрипции с промотор-
ными участками генов и переводу их из активных в "мол-
чащие" [Bogdan, 2001].
Еще один возможный неферментативный путь - нитро-
зилирование монооксидом азота S-белков кальциевых ка-
налов, что приводит к их открыванию и повышает концен-
трацию ионов кальция в цитозоле [Klausner et al., 1997]. Так
же как и в случае белков кальциевых каналов, нитрозили-
рование цитозольных S-белков может привести к измене-
нию их конформации, а это, в свою очередь, - к атакуемо-
сти протеазами и изменению времени жизни S-белков.
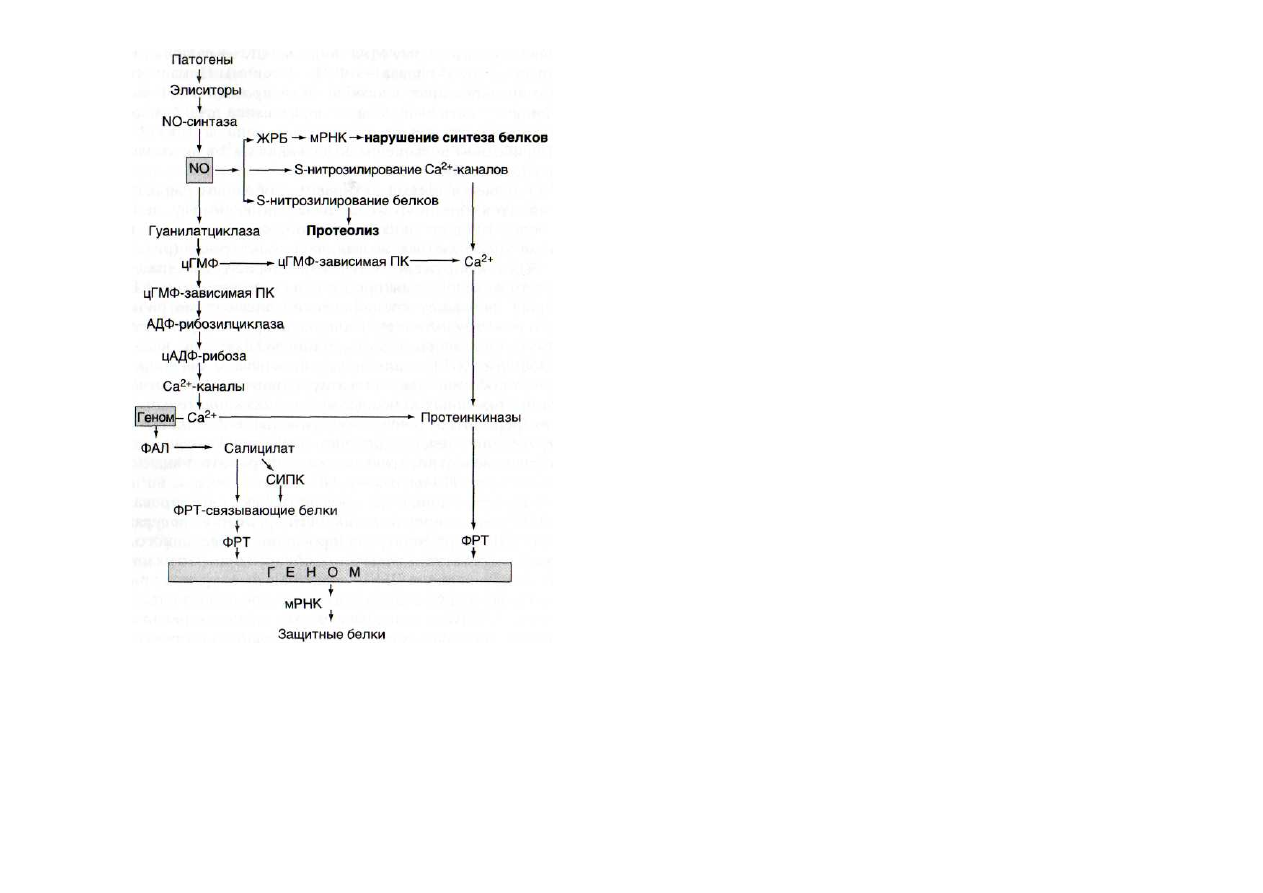
Рис. 33. Схема NO-синтазной сигнальной системы, дополнен-
ная неферментативным влиянием NO на метаболические про-
цессы
ЖРБ - железорегуляторный белок; ПК - протеинкиназа; СИПК -
салицилатиндуцируемая протеинкиназа; ФАЛ - фенилаланин-аммиак-
лиаза; ФРТ - факторы регуляции транскрипции
N0 и образующийся из него пероксинитрит могут окис-
лять тиоловые остатки в белках с образованием сульфено-
вых R-SOH-, сульфиновых R-SO
2
H-
и сульфоновых R-SO
3
H-
остатков [Bogdan, 2001]. В результате окисления тиоловых
остатков сульфгидрильные группы могут окисляться до ди-
сульфидных. Обнаружено, что под влиянием NO происхо-
дит разрушение кластеров ZnS в "цинковых пальцах" фак-
торов регуляции транскрипции, и это приводит к повыше-
нию концентрации ионов цинка в цитозоле и ядре.
Неферментативными путями вмешательства N0 в бел-
ковый метаболизм тканей растений могут быть объяснены
данные о влиянии донора NO - нитропруссида, на набор
белков, полученные в нашей лаборатории В.Г. Яковлевой.
Введение в проростки гороха нитропруссида привело уже
через сутки после начала опыта к изменению набора поли-
пептидов в растениях. Исчезли характерные для контроль-
ных растений полипептиды 19 и 30 кДа и появились новые
с молекулярными массами 32 и 36 кДа.
Проростки гороха уже давно стали для нашей лабора-
тории модельным объектом, с помощью которого мы ис-
следовали влияние на набор и содержание белков салици-
ловой [Тарчевский и др., 1996а, б; 1999; 2001], янтарной
|Тарчевский и др., 1999], абсцизовой [Тарчевский и др.,
2001], жасмоновой [Тарчевский и др., 1996а, б] кислот, а
также инфицирования микоплазмами [Тарчевский и др.,
1996а, б]. Во всех случаях наблюдаемое изменение набора
полипептидов в растениях отмечалось лишь через несколько
дней после начала воздействия того или иного исследуемого
соединения. Через сутки после начала воздействия на
проростки гороха салициловой кислоты не произошло из-
менения набора полипептидов, наблюдалось лишь некото-
рое относительное (по сравнению с контрольными расте-
ниями) повышение содержания полипептида 34 кДа, Бы-
строе салицилатнезависимое появление этого полипепти-
да, вызванное донором NO нитропруссидом, могло объяс-
няться неферментативной активацией матричной РНК с
помощью монооксида азота.
Ранее [Durner et al., 1998; Klessig et a!., 2000] было уста-
новлено, что NO вызывал достаточно быстрое появление
двух белков - PR 1 и фенилаланин-аммиак-лиазы - менее
чем через 24 ч после начала воздействия, но эти результаты
были получены в опытах с использованием более чувстви-
тельного метода иммуноблотинга.
Быстрое NO-индуцированное салицилатнезависимое ис-
чезновение полипептидов 19 и 30 кДа в опытах, проведенных
в нашей лаборатории, можно было бы объяснить прекраще-
нием их синтеза. Но это происходило бы лишь в том случае,
если скорость их оборота была бы очень велика. Возможно,
что непосредственное взаимодействие NO с этими белками
приводило к изменению их конформации и, вследствие это-
го, к быстрой деградации с помощью протеаз.
Примечателен тот факт, что многократное повышение
(всплеск) содержания цГМФ, вызванное N0, было преходя-
щим [Dinner et al., 1998], но синтез NO-индуцированных белков
продолжался, что свидетельствует о гораздо большем време-
ни жизни более поздних звеньев этого сигнального пути.
Остается неясным, что в NO-синтазой системе является
рецептором элиситоров, расположены они в плазмалемме
или цитозоле и принимают ли участие G-белки в качестве
промежуточного звена между рецептором и NO-синтазой?
Ответа на этот вопрос не содержится ни в статьях журнала
"Биохимия" [1998. Т. 63, вып. 7], специально посвященного
N
0, ни в пока еще немногочисленных статьях о сигнальной
функции NO у растений. Возникает вопрос: не является ли
рецептором сама молекула фермента NO-синтазы? К этому
предположению склоняют ее сложность и присутствие в до-
менах регуляторных цистеиновых сайтов, изменение актив-
ности в ответ на различные эффекторы, такие как цитоки-
ны у животных, на фосфорилирование, существование не-
большого эндогенного белкового ингибитора, препятству-
ющего образованию активной димерной формы фермента.
Интересно, что мутантные мыши, лишенные каждая одной
из изоформ NO-синтазы, оказались жизнеспособными, но
обнаруживали ряд особенностей в поведении. Кроме того,
мыши, дефектные по индуцибельной NO-синтазе, были бо-
лее чувствительны к инфекциям [Snyder, 1995].
Интенсивные исследования функционирования NO-син-
тазной сигнальной системы у растений должны в ближай-
шем будущем привести к новым интересным фактам, каса-
ющимся локализации ферментов этой системы, регуляции
их активности, взаимоотношений с другими сигнальными
системами и т.д.
ПРОТОННАЯ СИГНАЛЬНАЯ СИСТЕМА
При анализе участия различных сигнальных систем в за-
щитных реакциях против патогенов (образование фитоале-
ксинов и т.д.) необходимо учитывать, что одна из наиболее
ранних и неопровержимо доказанных реакций клеток на
действие элиситоров, учитываемых с помощью селектив-
ных электродов или флуоресцирующих рН-индикаторных
красок, - быстрое преходящее изменение в цитозоле кон-
центрации протонов за счет входа Н
+
из вакуоли и внекле-
точной среды [Conrath et al., 1991; Mathieu et al., 1991; 1994;
1996; Horn et al., 1992; Nurnberger et al., 1994; Hahlbrock et al.,
1995; Amano et al., 1997; Jabs et al., 1997; Roos et al., 1998].
Трансмембранное передвижение протонов происходит по
градиенту концентрации за счет того, что с внешней сторо-
ны плазмалеммы среда более кислая, чем с внутренней, и
разница может достигать двух единиц рН.
Так, в культуре клеток табака происходили подкисление
цитозоля и подщелачивание инкубационной среды, вызван-
ное олигогалактуронидами [Mathieu et al., 1991]. Подкисле-
ние цитозоля и подщелачивание среды наблюдались в сус-
пензионных клетках табака не только при действии олиго-
галактуронидов, но и криптогеина и других элиситоров
[Mathieu et al.,
1996], причем интенсивность и кинетика сдви-
га рН зависела от вида элиситоров, связывающихся с рецеп-
торами плазмалеммы. Механизм преобразования элиситор-
ных сигналов, приводящий к открыванию протонных кана-
лов, продолжает оставаться невыясненным. Совершенно
очевидно, что необходимым звеном этого механизма явля-
ется фосфорилирование белков Н
+
-
каналов [Mathieu et al.,
1996]. Показано, что ингибиторы протеинкиназ, например
стауроспорин, подавляли элиситориндуцируемое подкисле-
ние цитозоля, а ингибитор протеинфосфатаз каликулин А