ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 27.11.2019
Просмотров: 4035
Скачиваний: 98
Время после повреждения, мин
Рис. 9. Активация МАР-киназы механическим повреждением трех-
месячного растения табака путем срезания стебля под первым
снизу листом [Seo et al., 1999]
После срезания стебля в этом листе исследовали в течение 60 мин ак-
тивность МАР-киназы (в контрольных растениях принятую за единицу)
kinases -
индуцируемые механическим повреждением и са-
лицилатиндуцируемые протеинкиназы). Оказалось, что ак-
тивация WIPK осуществляется не только при повреждении
тканей растений, но и при их инфицировании вирусом та-
бачной мозаики [Zhang, Klessig, 1998a], а активация SIPK -
при действии олигосахаридных элиситоров и белковых эли-
ситинов [Zhang et al., 1998].
Активация МАР-киназ носит преходящий характер
(рис. 9), наподобие того, что происходит с ферментами и ин-
термедиатами других сигнальных систем [Seo et al., 1999].
Интересно, что ранаактивируемая МАР-киназа вызы-
вает накопление жасмоната и метилжасмоната, по-види-
мому, вследствие активации ФЛА
2
. Участие МАР-киназной
сигнальной системы в активации липоксигеназного сиг-
нального пути было подтверждено в специальных опытах
[Meindl et al.,
1998]. Так как интермедиаты липо-
ксигеназного метаболизма вызывают апоптоз клеток рас-
тений, то не вызывает удивления, что в нем принимает
участие и элиситориндуцируемый МАР-киназный каскад
[Suzuki et al., 1999].
Обнаружена индукция образования транскриптов про-
теинкиназ МАРК-сигнальной системы (и связанная с этим
их активация) под влиянием различных стрессоров
[Mizoguchi et al.,
1996]. Чаще всего интермедиаты МАР-ки-
назной сигнальной системы активируются или инактивиру-
ются за счет посттрансляционной модификации, подверга-
ясь главным образом фосфорилированию [Romeis et
al.,1999]
или дефосфорилированию [Gupta et al., 1998;
Meskiene et al., 1998; Meskiene, Hirt,
2000] с помощью соот-
ветствующих протеинкиназ и протеинфосфатаз.
МАР-киназная сигнальная система активируется многи-
ми внеклеточными сигналами, что объясняется большим
разнообразием представителей стартового фермента в цепи
киназ. Все МАРКК-киназы (МАРККК) подразделяются на
четыре группы [Widmann et al., 1999; Meskiene, Hirt, 2000] в
зависимости от особенностей первичной структуры, о кото-
рой стало возможным судить после клонирования соответ-
ствующих генов. Различия касаются в первую очередь стру-
ктуры регуляторного домена, но они обнаружены также в
других доменах, таких, например, как zinc zipper (цинковая
застежка-молния), лейциновые "застежки", места связыва-
ния G-белков, несколько мест фосфорилирования тирози-
новых, сериновых и треониновых остатков. Как уже отме-
чалось, в соответствии с разнообразием структуры
МАРКК-киназ представители этого семейства могут акти-
вироваться различными источниками сигналов. Это могут
быть другие протеинкиназы - ПКС и МАРКККК, различ-
ные G-белки семейств Ras и Rho. MAPKK имеет более огра-
ниченные возможности регуляции в связи с меньшей вариа-
бильностью структурных элементов этих ферментов.
В еще большей степени это касается МАРК. МАРККК ка-
тализирует фосфорилирование остатков серина и треонина
в МАРКК, а последняя - остатков треонина и тирозина в
МАРК. По всей вероятности, МАРКК активирует (путем
фосфорилирования) лишь МАРК. Можно сделать вывод,
что в случае с каскадом МАРККК -» МАРКК -» МАРК мы
имеем дело с сигнальной "воронкой", с конвергенцией сиг-
нальных путей, инициируемых в пределах МАРК-системы
различными элиситорами. В этом случае последнее звено
этой системы - МАР-киназа, может активировать лишь
один тип факторов регуляции транскрипции, вызывая экс-
прессию более узкого круга генов, чем можно было бы
ожидать, если иметь в виду большое разнообразие
МАРККК. МАР-киназа может также катализировать фос-
форилирование цитоскелетных белков и фосфолипаз, ак-
тивируя их.
К 2000 г. были клонированы гены 17 представителей
МАРККК, МАРКК и 28 представителей МАР-киназ из раз-
личных видов растений [Ligterink, 2000]. Вполне вероятно,
что во взаимодействии этих протеинкиназ определенную
роль играют комплексообразующие белки типа scaffold pro-
teins.
Как уже отмечалось выше, активация сигнальных сис-
тем носит преходящий характер, а это означает, что долж-
ны быть эффективные механизмы их самоингибирования.
Инактивация МАР-киназной сигнальной системы осущест-
вляется, в первую очередь, за счет дефосфорилирования
МАРК с помощью протеинфосфатаз. Все имеющие отно-
шение к МАР-сигнальному каскаду протеинфосфатазы
подразделяются на три группы [Meskiene, Hirt, 2000]: фер-
менты двойной специфичности, осуществляющие дефосфо-
рилирование остатков тирозина и треонина в МАР-киназах,
тирозиновые протеинфосфатазы и серин-треониновые
протеинфосфатазы.
ФОСФАТИДАТНАЯ СИГНАЛЬНАЯ СИСТЕМА
Следующие три раздела посвящены сигнальным систе-
мам, функционирование которых начинается с превраще-
ния мембранных фосфолипидов, катализируемого различ-
ными фосфолипазами: ФЛД, ФЛС и ФЛА
2
. Изначально счи-
талось, что их активация является главной причиной обно-
вления мембранных фосфолипидов при изменении условий
существования растений, замены ранее существовавших ли-
пидов на более соответствующие новым условиям. В каче-
стве примера можно привести замену фосфолипидов с низ-
ким содержанием ненасыщенных жирных кислот на фос-
фолипиды с высоким их содержанием при понижении тем-
пературы. Со временем удалось установить еще одну чрез-
вычайно важную функцию фосфолипаз: запуск по крайней
мере трех сигнальных систем - фосфатидатной, кальциевой
и липоксигеназной.
В последние годы все большее внимание уделяется сиг-
нальной системе, "включаемой" активацией фосфолипаз Д
под влиянием патогенов, элиситоров и при абиотическом
стрессе [Munnik et al., 1998; Wang, 1999] (рис. 10). Так как
при этом происходит освобождение из фосфолипидов фос-
фатидной кислоты, то эта сигнальная система получила на-
звание фосфатидатной [Тарчевский, 2000].
Фосфолипазы Д представляют собой достаточно гете-
рогенное семейство белков [Qin et al., 1997; X. Wang, 2000] с
большой протяженностью консервативных последователь-
ностей аминокислот и с отличающимися участками струк-
туры, отвечающими за особенности регуляции каждой из
изоформ этого фермента, например за степень активации
ионами кальция, инозитолполифосфатами или механиче-
ским повреждением тканей [С. Wang, 2000]. Интересно, что
последнее воздействие вызывало наивысшую активацию
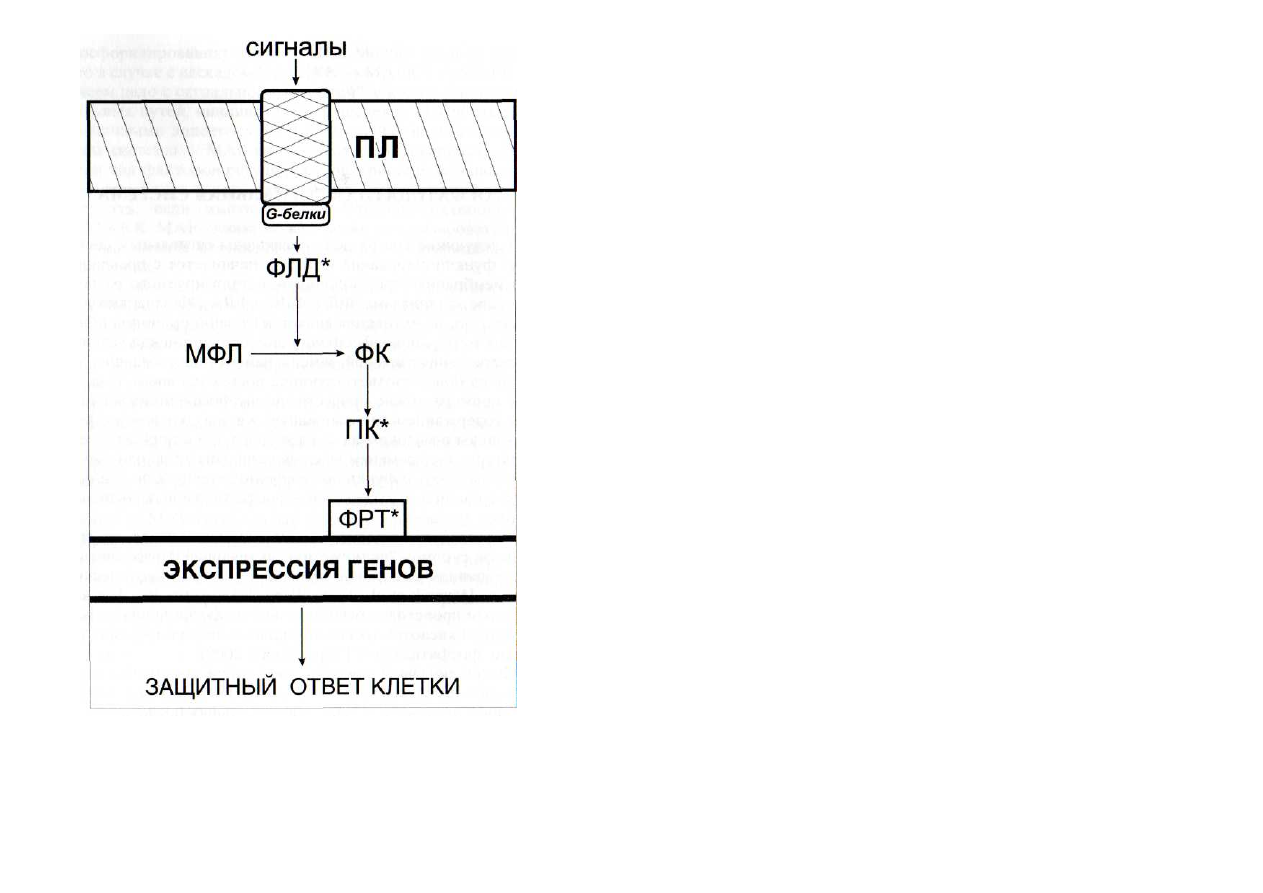
Рис. 10. Схема функционирования фосфатидатной сигнальной системы
МФЛ - мембранные фосфолипиды; ПК - протеинкиназа; ФК - фос-фатидная
кислота; ФЛД - фосфолипаза Д. Остальные обозначения -см. рис. 6
предсуществующих молекул фермента у той изоформы фо-
сфолипазы Д, для которой была характерна наименьшая
экспрессия генов. По всей вероятности, эта изоформа отвечает
за наиболее быстрые сигнальные события, а другие изоформы
-
за более поздние, поскольку на синтез ферментов de novo
требуется затрата гораздо большего времени.
Лучшими субстратами для фосфолипаз Д являются фо-
сфатидилхолин, фосфатидилэтаноламин и фосфатидил-
глицерол. Обнаружено, что патогены и механическое по-
вреждение вызывают передвижение ФЛД из цитозоля к
плазмалемме и повышение активности фермента (рис. 11)
[Ryu, Wang,
1996]. Возможность связывания с мембранами
некоторых изоформ фосфолипазы Д определяется их ми-
ристоилированием, что приводит к повышению гидрофоб-
ности. Привлекает внимание, что один из доменов ФЛД
способен связываться с Са
2+
и фосфолипидами и таким образом
регулировать транспорт фермента к мембране. Домен со
сходной структурой был обнаружен также у ряда других
белков, принимающих участие в функционировании
сигнальных систем клеток (у фосфолипаз С и А
2
, у
протеинкиназы С).
Повышают активность части фосфолипаз Д протеинкиназа
С, Са
2+
, тримерные G-белки и малые G-белки, полифо-
сфоинозитид; снижают активность лизофосфатиды. Было
обнаружено, что преходящее накопление фосфатидатной
кислоты происходило и без влияния элиситоров, если на
клетки воздействовали активатором G-белков мастопара-ном
[Munnik et al.,
1995], из чего следует, что в роли сигнального
интермедиата между рецептором элиситора и фосфо-липазой Д
выступает G-белок.
Различные изоформы фосфолипазы Д имеют отличаю-
щиеся оптимальные для проявления активности значения рН.
Особый интерес представляет одна из основных изоформ,
которая активируется повышающимися концентрациями
ионов кальция (оптимальные значения для этой изоформы - от
20 до 100 мМ) и подкислением среды (оптимальные значения
рН от 4,5 до 5,0), т.е. наиболее ранними изменениями в
клетках, которые создаются на внутренней поверхности
плазмалеммы и на внешней поверхности тоно-пласта при
действии на клетки растений различных элиситоров. Для
других изоформ оптимальными являются мик-
Время после механического повреждения растения, ч
Рис. 11. Влияние механического повреждения листьев арабидоп-сиса на
связывание фосфолипазы Д мембранами [X. Wang, 2000] 1 - фракция мембран
(осадок после центрифугирования при 100 000 g надосадочной жидкости,
полученной после центрифугирования гомогената листьев при 6000 g); 2 -
фракция растворимых соединений, содержащихся в надосадочной жидкости
после центрифугирования при 100 000 g. Проводился иммуноблоттинг
фосфолипазы Д
ромолярные концентрации ионов кальция и приближающиеся к
нейтральным значения рН.
Сначала у животных, а затем и у растительных объектов было
обнаружено, что свободная фосфатидная кислота является
липидным вторичным мессенджером, который способен
активировать ряд белков, включая малый (small) G-белок, Са2+-
зависимую и Са2+-независимую протеинкина-зы, МАР-киназы,
НАДФН-оксидазу, фосфолипазы С и А2 [Wang, 1999; Sang et al.,
2001].
В фосфатидатной системе стимуляция элиситором фосфолипазы
Д, опосредованная активацией G-белка мастопа-
раном, приводит к освобождению из фосфолипидов плазма-
леммы фосфатидной кислоты, которая выступает в роли
вторичного посредника, от которого сигнальный импульс
передается на протеинкиназы и затем на факторы регуляции
транскрипции, вызывая в конечном итоге экспрессию
защитных генов.
Установлено, что фосфатидат способен превращаться в
интермедиаты, характерные для других сигнальных путей: в
диацилглицерол кальциевого пути, а также в полиеновые
жирные кислоты и лизофосфатидную кислоту липоксиге-
назного пути.
Оказалось также, что накопление свободной фосфатидной
кислоты может изменять свойства мембран и, вследствие этого,
активность связанных с ними участников других сигнальных
систем. Обращает на себя внимание, что фосфатидная кислота
является кальциевым ионофором, из чего следует, что она
может оказывать некоторое влияние на функционирование
кальциевой сигнальной системы.
КАЛЬЦИЕВАЯ СИГНАЛЬНАЯ СИСТЕМА
Повышение концентрации ионов кальция в цитозоле является
одной из наиболее ранних ответных реакций на инфицирование
патогенами (на действие элиситоров), на механическое
повреждение (или раздражение) и другие стрессоры. Эта
кальциевая "вспышка" носит преходящий характер. Ее
восходящая ветвь вызвана открыванием кальциевых каналов,
расположенных в плазмалемме, вакуолярном тонопласте и в
мембранах эндоплазматической сети [Blume et al., 2000]. Во всех
трех случаях имеет место чрезвычайно высокий трансмембранный
электрохимический градиент Са
2+
-
в цитозоле концентрация этих
ионов при невозбужденном состоянии клетки приблизительно в
1000 раз меньше, чем в клеточной стенке, вакуоле или в матриксе
эндоплазматической сети, и цитозольная сторона мембран заря-
жена отрицательно по сравнению с другой стороной. При
открывании кальциевых каналов ионы кальция устремляются в
цитозоль, и их концентрация повышается в 10-20 раз. Эта
кальциевая "вспышка" используется клеткой в качестве
сигнального интермедиата. В основе сигнальной функции лежит
способность ионов кальция взаимодействовать с белками. При
связывании ионов кальция некоторыми остатками аминокислот,
например аспартата или глута-мата, происходит изменение
заряда соответствующего участка белка и, вследствие этого,
конформации белковой молекулы. Это сказывается на ее
активности, что и используется для передачи элиситорного
сигнала на последующие звенья сигнальных цепей.
Так же как и в большинстве других сигнальных систем, в
случае кальциевой системы элиситоры связываются с ре-
цепторами плазмалеммы (рис. 12), после чего элиситорный
импульс трансмембранно передается на комплекс G-бел-
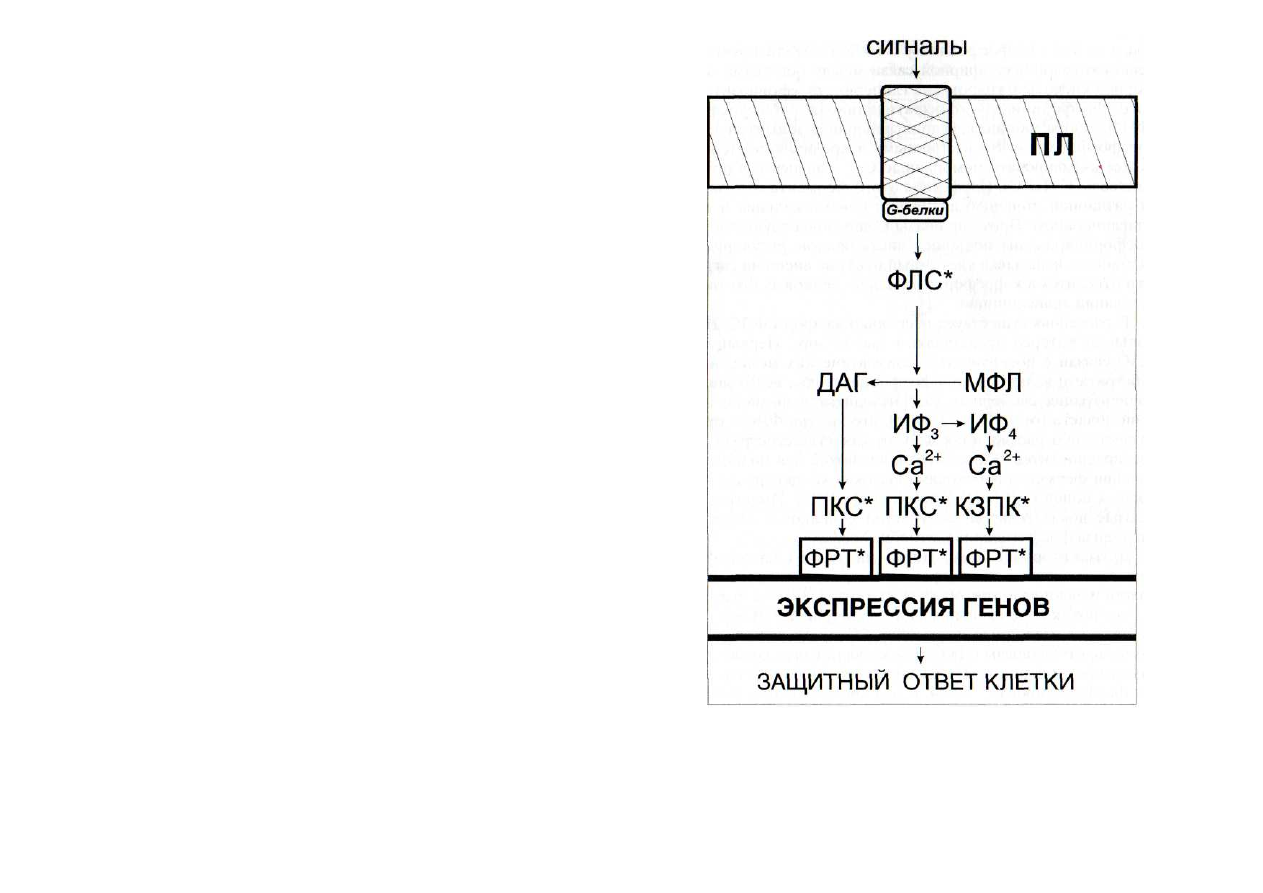
Рис. 12. Схема функционирования кальциевой сигнальной си-
стемы
ДАГ - диацилглицерол; ИФ
3
-
инозитолтрисфосфат; ИФ
4
-
инози-
толтетракисфосфат; КЗПК - кальцийзависимая протеинкиназа, отличная от
ПКС; МФЛ - мембранные фосфолипиды; ПКС - протеинкина-зы С; ФЛС -
фосфолипаза С. Остальные обозначения - см. рис. 6