Файл: Билеты по общей и неорганической химии для студентов 125Ф3 озо (20222023учебный год) Билет 1.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 07.11.2023
Просмотров: 308
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
й одная кислота (HIO4) степень окисления +7
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
Билеты по общей и неорганической химии для студентов 125Ф3 ОЗО (2022-2023учебный год)
Билет № 1
-
Характеристика кальция, магния, и их соединений. Биологическая роль кальция. Применение в медицине и народном хозяйстве.
Щелочноземельные металлы расположены во второй группе главной подгруппе периодической системы химических элементов Менделеева. На практике к щелочноземельным металлам относят кальций Ca, а магний Mg проявляет некоторые свойства щелочноземельных металлов, но в целом отличается от них.
Э
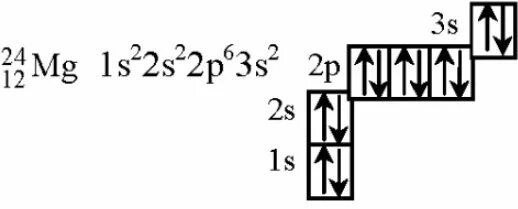 лектронная конфигурация внешнего энергетического уровня щелочноземельных металлов: ns2, на внешнем энергетическом уровне в основном состоянии находится 2 s-электрона. Следовательно, типичная степень окисления щелочноземельных металлов в соединениях +2.
лектронная конфигурация внешнего энергетического уровня щелочноземельных металлов: ns2, на внешнем энергетическом уровне в основном состоянии находится 2 s-электрона. Следовательно, типичная степень окисления щелочноземельных металлов в соединениях +2.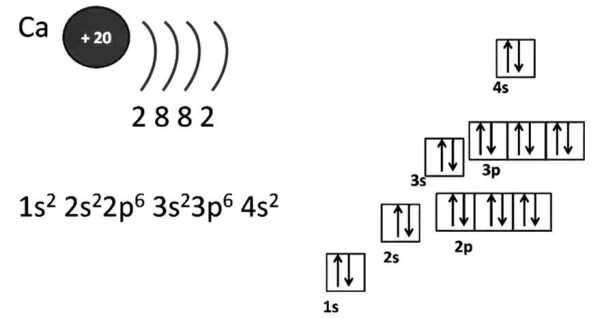
Все щелочноземельные металлы — вещества серого цвета и гораздо более твердые, чем щелочные металлы.
Магний и кальций (Mg и Ca) устойчивы в сухом воздухе.
Кристаллическая решетка щелочноземельных металлов, к которым относятся магний и кальций, в твёрдом состоянии — металлическая. Следовательно, они обладают высокой тепло- и электропроводимостью. Кипят и плавятся при высоких температурах.
Нахождение в природе
Как правило, щелочноземельные металлы в природе присутствуют в виде минеральных солей: хлоридов, бромидов, йодидов, карбонатов, нитратов и др.
Основные минералы, в которых присутствуют щелочноземельные металлы:
Доломит — CaCO3 · MgCO3 — карбонат кальция-магния.

Магнезит MgCO3 – карбонат магния.

Кальцит CaCO3 – карбонат кальция.

Гипс CaSO4 · 2H2O – дигидрат сульфата кальция.

Способы получения
Магнийполучают электролизом расплавленного карналлита или хлорида магния с добавками хлорида натрия при 720–750°С:
MgCl2 → Mg + Cl2
или восстановлением прокаленного доломита в электропечах при 1200–1300°С:
2(CaO · MgO) + Si → 2Mg + Ca2SiO4
Кальцийполучают электролизом расплавленного хлорида кальция с добавками фторида кальция:
CaCl2 → Ca + Cl2
Качественные реакции
Качественная реакция на щелочноземельные металлы — окрашивание пламени солями щелочноземельных металлов. Цвет пламени: Ca — кирпично-красный.
Качественная реакция на ионы магния: взаимодействие с щелочами. Ионы магния осаждаются щелочами с образованием белого осадка гидроксида магния:
Mg2+ + 2OH— → Mg(OH)2↓
Качественная реакция на ионы кальция - взаимодействие с карбонатами. При взаимодействии солей кальция с карбонатами выпадает белый осадок карбоната кальция:
Ca2+ + CO32- → CaCO3↓
Также осадки белого цвета
образуются при взаимодействии солей кальция с сульфитами и фосфатами.
Например, при взаимодействии хлорида кальция с фосфатом натрия образуется белый осадокфосфата кальция:
3CaCl2 + 2Na3PO4 → 6NaCl + 2Ca3(PO4)2↓
Химические свойства
1. Щелочноземельные металлы — сильные восстановители. Поэтому они реагируют почти со всеми неметаллами.
1.1. Щелочноземельные металлы реагируют с галогенами с образованием галогенидов при нагревании.
Например, кальций взаимодействует с хлором с образованием хлорида кальция:
Ca + Cl2 → CaCl2
Реакция кальция и хлора протекает при условии: при температуре 200-400 °C.
1.2. Щелочноземельные металлы реагируют при нагревании с серой и фосфором с образованием сульфидов и фосфидов.
Например, кальций взаимодействует с серой при нагревании:
Ca + S → CaS
Кальций взаимодействует с фосфором с образованием фосфидов:
3Ca + 2P → Ca3P2
1.3. Щелочноземельные металлы реагируют сводородом при нагревании. При этом образуются бинарные соединения — гидриды. Магний с водородом реагирует лишь при повышенном давлении.
Mg + H2 → MgH2
1.4. С азотоммагний взаимодействует при нагревании с образованием нитрида:
3Mg + N2 → Mg3N2
Кальций также реагируют с азотом при нагревании.
1.5. Щелочноземельные металлы реагируют с углеродом с образованием карбидов, преимущественно ацетиленидов.
Например, кальций взаимодействует с углеродом с образованием карбида кальция:
Ca + 2C → CaC2
Магнийи кальций горят на воздухе при 650°С с выделением большого количества света. При этом образуются оксиды и нитриды:
2Mg + O2 → 2MgO
3Mg + N2 → Mg3N2
2. Щелочноземельные металлы взаимодействуют со сложными веществами:
2.1. Щелочноземельные металлы реагируют с водой. Взаимодействие с водой приводит к образованию щелочи и водорода. Магний реагирует с водой при кипячении. Кальций реагируют с водой при комнатной температуре.
Например, кальцийреагирует с водой с образованием гидроксида кальция и водорода:
Ca0 + 2H2+O → Ca+(OH)2 + H20
2.2. Щелочноземельные металлы, магний и кальций, взаимодействуют с минеральными кислотами (с соляной, фосфорной, разбавленнойсерной кислотой и др.). При этом образуются соль и водород.
Например, магний реагирует с соляной кислотой:
Mg + 2HCl → MgCl2 + H2↑
2.3. При взаимодействии щелочноземельных металлов с концентрированной серной кислотойобразуется сера.
Например, при взаимодействии кальция с концентрированной серной кислотой образуется сульфат кальция, сера и вода:
4Ca + 5H2SO4(конц.) → 4CaSO4 + S + 5H2O
2.4. Щелочноземельные металлы реагируют с азотной кислотой. При взаимодей-ствии кальция и магния с концентрированной или разбавленной азотной кислотой образуется оксид азота (I):
4Ca + 10HNO3 (конц) → N2O + 4Сa(NO3)2 + 5H2O
При взаимодействии щелочноземельных металлов с очень разбавленной азотной кислотой образуется нитрат аммония:
4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
2.5. Щелочноземельные металлы могут восстанавливать некоторые неметаллы (кремний, бор, углерод) из оксидов.
Например, при взаимодействии кальция с оксидом кремния (IV) образуются кремний и оксид кальция:
2Ca + SiO2 → 2CaO + Si
Магний горит в атмосфере углекислого газа. При этом образуется сажа и оксид магния:
2Mg + CO2 → 2MgO + C
2.6. В расплавещелочноземельные металлы могут вытеснять менее активные металлы изсолей и оксидов. Обратите внимание! В растворе щелочноземельные металлы будут взаимодействовать с водой, а не с солями других металлов.
Например, кальцийвытесняет медь из расплава хлорида меди (II):
Ca + CuCl2 → CaCl2 + Cu
Минералымагния:
MgCO3 × CaCO3 – доломит
MgCO3 – магнезит
KCl × MgCl2 × 6H2O – карналлит
MgSO4 × KCl × 3H2O – каинит
Минералы кальция:
CaCO3 - кальцит (известняк, мел, мрамор)
СaSO4 × 2H2O – гипс
Ca3(PO4)2 – фосфорит
3Ca3(PO4)2 × CaF2 – апатит
-
Биологическая роль кальция. Кальций является одним из основных минералов в организме человека. Он принимает участие во многих биологических процессах. Макроэлемент необходим для формирования костной ткани и зубов, биологического синтеза гормонов, регуляции сосудистого тонуса деятельности сердечно - сосудистой системы. Он также необходим для реализации процесса свертываемости крови при повреждениях.
-
Применение соединений магния и кальция в медицине:
-
Жженая магнезия MgO применяется при повышенной кислотности желудочного сока, изжоге, отравлении кислотами. Входит в состав зубных порошков.
-
Горькая или английская соль MgSO4 × 7 H2O при приеме внутрь служит надежным и быстродействующим слабительным, а при внутримышечных или внутривенных вливаниях снимает судорожное состояние, уменьшает спазмы сосудов.
-
Как желчегонное его вводят в 12-перстную кишку.
-
CaCl2 × 6H2O хлорид кальция широко применяется в медицине как кровоостанавливающее средство при легочных, желудочных, кишечных и других кровотечениях, в хирургической практике для повышения свертываемости крови, при аллергических заболеваниях для снятия зуда и в качестве противоядия при отравлении солями магния.
-
Гипс CaSO4 × 0,5H2O в медицине находит применение для изготовления фиксирующих гипсовых повязок, а также в стоматологической практике для снятия слепков с челюстей при изготовлении искусственных зубов.
-
Кальций входит в состав препаратов для профилактики остеопороза, в витаминные комплексы для беременных и пожилых.
-
Применение магния и кальция в народном хозяйстве:
-
Соли магния и кальция вносят в почвы для химической мелиорации. Целями химической мелиорации являются устранение избыточной кислотности почв, вредной для многих сельскохозяйственных культур (известкование), и устранение избыточной щелочности почв (гипсование).
-
Соединения магния и кальция в строительстве. Соединения кальция и магния широко используют в строительстве в качестве конструкционных (известняк), отделочных (мрамор) и вяжущих материалов (цемент, известь, гипс).
-
Кальций широко применяется в металлотермии при получении редкоземельных элементов.
-
Кальциевые гранулы используются для удаления следов воздуха из электровакуумных приборов.
-
Сплавы кальция со свинцом находят применение в аккумуляторных батареях и подшипниковых сплавах.
-
Магний применяется для металлотермического получения некоторых тугоплавких металлов (титана, циркония).
-
Магний используется для получения легких сплавов (самолетостроение, производство автомобилей), для изготовления осветительных и зажигательных ракет.
-
Какие из указанных веществ имеют металлическую связь: Zn, S, C, KH, FeCl3, K, Ag, NaCl.
металлическую связь имеют: Zn, K, Ag.
Билет № 2
-
Галогены, биологическая роль и их применение в медицине.
В подгруппу галогенов входят элементы: фтор (F), хлор (Cl), бром (Br), йод (I) и астат (At).
Галогены находят широкое применение в практике. Все они, за исключением астата, используются для приготовления многочисленных органических и неорганических соединений; многие из них широко применяются в медицине как медикаменты и дезинфицирующие вещества. Все они, особенно хлор и йод, играют значительную роль в обмене веществ в организме человека, животных и растений. С увеличением порядкового номера галогена наблюдается повышение способности их к образованию биологически активных органических соединений.
Фтор относится к биомикроэлементам. Он играет значительную роль в развитии и минерализации костей и зубов; относится к абсолютно необходимым для организма микроэлементам. В медицине некоторые фторсодержащие соединения применяют как лекарственные средства, в т. ч. используемые для наркоза, в качестве кровезаменителей и др. Недостаточное поступление Фтора в организм является одним из экзогенных атиологических факторов кариеса зубов, особенно в период их прорезывания и минерализации. Фтор стимулирует репаративные процессы при переломах костей, предупреждает развитие сенильного остеопороза. Есть данные, что Фтор снижает накопление стронция в костной ткани и уменьшает тяжесть вызываемых радиоактивным стронцием поражений. Избыточное поступление фтора в организм является причиной возникновения флюороза, который поражает в основном постоянные зубы людей.
Хлор элемент входит в состав желудочного сока, препаратов для лечения ряда желудочно-кишечных заболеваний. В медицинской практике препараты хлора используют главным образом как дезинфицирующие средства и антисептические средства.
Анионы хлора являются наиболее важными осмотически активными ионами крови, лимфы, клеточного содержимого, цереброспинальной жидкости.
Хлор используется для хлорирования водопроводной воды, уничтожения болезнетворных бактерий, для производства хлорсодержащих веществ.
Бром используется в медицине, при лечении неврозов, истерии, бессонницы и других расстройств нервной системы, широко применяются бромиды калия, натрия, кальция и аммония, а также некоторые органические соединения брома (напр., бромкамфора, бромизовал и др.). Чрезмерное накопление в организме бромистых солей (бромизм) вызывает кожные сыпи и угнетение нервной системы.
Бромиды – группа препаратов, содержащих бром и обладающих седативными свойствами.
В диагностике при исследовании обмена воды и электролитов, применяется нейтральный изотонический, апирогенный и стерильный раствор бромида натрия.
Йод в норме, в теле человека содержится приблизительно 25 мг% йода, половина этого количества накапливается в виде сложного белка — тиреоидина в щитовидной железе.
Среди препаратов йода, применяемых в медицинской практике, различают:
-
препараты, содержащие элементарный (свободный) йод - раствор йода спиртовой, раствор Люголя;
-
препараты, способные освобождать элементарный йод - йодинол, йодофор, кальцийодин;
-
препараты, диссоциирующие с образованием ионов йода (йодиды) - калия йодид и натрия йодид;
-
препараты, содержащие прочно связанный йод - йодолипол, билитраст и другие рентгеноконтрастные вещества;
-
радиоактивные препараты йода.
Влияние препаратов йода на обмен веществ проявляется усилением процессов диссимиляции. При атеросклерозе они вызывают некоторое снижение концентрации холестерина и липопротеидов в крови; кроме того, повышают фибринолитическую и липопротеиназную активность сыворотки крови и замедляют скорость свертывания крови.
Препараты йода используют для наружного и внутреннего применения. Наружно применяют гл. обр. препараты элементарного йод в качестве раздражающих и отвлекающих средств. Кроме того, эти препараты и препараты, отщепляющие элементарный йод применяют в качестве антисептических средств.
Внутрь препараты йода назначают при гипертиреозе, эндемическом зобе, третичном сифилисе, атеросклерозе, хронической интоксикациях ртутью и свинцом.
Йодиды, кроме того, назначают внутрь в качестве отхаркивающих средств.
Астат при попадании в организм концентрируется в печени. Как и йод, астат способен накапливаться в щитовидной железе. α-излучение астата поражает близлежащие ткани, приводит к нарушению их функции и в перспективе — к образованию опухолей. Кроме того, частичное накопление астата наблюдается в молочных желёзах.
Неустойчивость астата делает применение его соединений проблематичным, тем не менее изучалось возможность использования различных изотопов этого элемента для борьбы с онкологическими заболеваниями.
-
К солям относятся следующие соединения: KCl, CaS, LiHSO4, CuOH, NaOH, Al(OH)3, H[AuCl4], Na3[AlF6], H2[ZnCl4], CaO, MgO, ZnO. Назовите их.
KCl – хлорид калия, калий хлористый, сильвин
CaS – сульфид кальция
LiHSO4 – гидросульфат лития, кислая соль лития
Na3[AlF6] – Гексафтороалюминат натрия, смешанная соль
Билет № 3
-
Общая характеристика халькогенов. Характеристика кислорода. Соединения кислорода с водородом. Применение в медицине и народном хозяйстве.
-
Халькогены — это элементы VIA группы. Родоначальником этой группы является кислород. Кроме кислорода O в эту группу входят S, Se, Te, Po. Название халькогены означает «рождающие руды».
На внешнем энергетическом уровне у халькогенов 6 электронов. До завершения внешнего энергетического уровня атомам не хватает 2 электрона, поэтому они присоединяют электроны и проявляют в своих соединениях степень окисления -2. Кислород в соединении с фтором — OF2 проявляет степень окисления +2. Атомы серы, селена и теллура в своих соединениях с более электроотрицательными элементами проявляют положительные степени окисления +2, +4 и +6.
-
Кислород — самый распространенный элемент на Земле. Он входит в состав воды, которая покрывает поверхность земного шара, образуя его водную оболочку — гидросферу. Кислород входит в состав атмосферы, где на его долю приходится 21%. Кроме этого, он ещё входит в состав многих органических соединений.
Кислород образует две аллотропных модификации — кислород O2 и озон O3 , которые отличаются составом молекул и обладают разными свойствами. Кислород содержится в воздухе, он необходим для дыхания, а также для горения топлива и других веществ. Кислород — газ без цвета и запаха. При температуре – 1830C кислород сжижается, а при - 2190C переходит в твёрдое состояние. Жидкий кислород имеет голубую окраску, а твёрдый кислород - синюю.
Озон O3 — бесцветный газ с характерным запахом, содержится в верхних слоях атмосферы и защищает Землю от жёсткого ультрафиолетового излучения Солнца. В отличие от кислорода, озон чрезвычайно ядовит. Озон неустойчив и легко превращается в кислород.
Электронная конфигурация кислородав основном состоянии:
+8O 1s22s22p4 1s 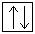 2s
2s  2p
2p 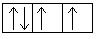
Атом кислорода содержит на внешнем энергетическом уровне 2 неспаренных электрона и 2 неподеленные электронные пары в основном энергетическом состоянии.
Способы получения
В промышленностикислород получают перегонкой жидкого воздуха.
Лабораторные способы получения кислорода:
-
Разложение некоторых кислородосодержащих веществ:
Разложение перманганата калия:
2KMnO4 → K2MnO4 + MnO2 + O2
Разложение бертолетовой соли в присутствии катализатора MnO2:
2KClO3 → 2KCl + 3O2
Разложение пероксида водорода в присутствии оксида марганца (IV):
2H2O2 → 2H2O + O2
2HgO → 2Hg + O2
2KNO3 → 2KNO2 + O2
Химические свойства
При нормальных условиях чистый кислород — очень активное вещество, сильный окислитель. В составе воздуха окислительные свойства кислорода не столь явно выражены.
1. Кислород проявляет свойства окислителя (с большинством химических элементов) и свойства восстановителя (только с более электроотрицательным фтором). В качестве окислителя кислород реагирует и с металлами, и с неметаллами. Большинство реакций сгорания простых веществ в кислороде протекает очень бурно, иногда со взрывом.
1.1. Кислород реагирует с фторомс образованием фторидов кислорода:
O2 + 2F2 → 2F2O
С хлором и бромом кислород практически не реагирует, взаимодействует только в специфических очень жестких условиях.
1.2. Кислород реагирует с серой и кремнием с образованием оксидов:
S + O2 → SO2
Si + O2 → SiO2
1.3. Фосфор горит в кислороде с образованием оксидов:
При недостатке кислорода возможно образование оксида фосфора (III):
4P + 3O2 → 2P2O3
Но чаще фосфор сгорает до оксида фосфора (V):
4P + 5O2 → 2P2O5
1.4. С азотом кислород реагирует при действии электрического разряда, либо при очень высокой температуре (2000оС), образуяоксид азота (II):
N2 + O2 → 2NO
1.5. В реакциях с щелочноземельными металлами, литием и алюминием кислород также проявляет свойства окислителя. При этом образуются оксиды:
2Ca + O2 → 2CaO
Однако при горении натрия в кислороде преимущественно образуется пероксид натрия:
2Na + O2 → Na2O2
А вот калий, рубидий и цезий при сгорании образуют смесь продуктов, преимущес-твенно надпероксид:
K + O2→ KO2
Переходные металлы окисляются кислород обычно до устойчивых степеней окисления.
Цинк окисляется до оксида цинка (II):
2Zn + O2→ 2ZnO
Железо, в зависимости от количества кислорода, образуется либо оксид железа (II), либо оксид железа (III), либо железную окалину:
2Fe + O2 → 2FeO
4Fe + 3O2 → 2Fe2O3
3Fe + 2O2 → Fe3O4
1.6. При нагревании с избытком кислорода графит горит, образуя оксид углерода (IV):
C + O2 → CO2
при недостатке кислорода образуется угарный газ СО:
2C + O2 → 2CO
2. Кислород взаимодействует со сложными веществами:
2.1. Кислород окисляет бинарные соединения металлов и неметаллов: сульфиды, фосфиды, карбиды, гидриды. При этом образуются оксиды:
4FeS + 7O2→ 2Fe2O3 + 4SO2
Al4C3 + 6O2→ 2Al2O3 + 3CO2
Ca3P2 + 4O2→ 3CaO + P2O5
2.2. Кислород окисляет бинарные соединения неметаллов:
-
летучие водородные соединения (сероводород, аммиак, метан, силан гидриды). При этом также образуются оксиды:
2H2S + 3O2 → 2H2O + 2SO2
Аммиак горит с образованием простого вещества, азота:
4NH3 + 3O2 → 2N2 + 6H2O
Аммиак окисляется на катализаторе (например, губчатое железо) до оксида азота (II):
4NH3 + 5O2 → 4NO + 6H2O
-
прочие бинарные соединения неметаллов — как правило, соединения серы, углерода, фосфора (сероуглерод, сульфид фосфора и др.):
CS2 + 3O2→ CO2 + 2SO2
-
некоторые оксиды элементов в промежуточных степенях окисления (оксид углерода (II), оксид железа (II) и др.):
2CO + O2→ 2CO2
2.3. Кислород окисляет гидроксиды и соли металлов в промежуточных степенях окисления в водных растворах.
Например, кислород окисляет гидроксид железа (II):
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3
Кислород окисляет азотистуюкислоту:
2HNO2 + O2 → 2HNO3
2.4. Кислород окисляет большинство органических веществ. При этом возможно жесткое окисление (горение) до углекислого газа, угарного газа или углерода:
CH4 + 2O2 → CO2 + 2H2O
2CH4 + 3O2 → 2CO + 4H2O
CH4 + O2 → C + 2H2O
Также возможно каталитическое окисление многих органических веществ (алкенов, спиртов, альдегидов и др.)
2CH2=CH2 + O2 → 2CH3-CH=O
-
Соединения кислорода с водородом. Кислород образует с водородом два соединения: оксид водорода – воду (Н2О) 2Н2 + О2 → 2Н2О
и пероксид водорода (Н2О2) 2H2O + O2 → 2H2O2
С водородом кислород образует воду Н2О. В процессе этой реакции выделяется значительное количество теплоты.
Смесь двух объемов водорода с одним кислорода при поджигании взрывается; она носит название гремучего газа.
С водородом кислород образует соединение – пероксид водорода Н2О2 – бесцветная прозрачная жидкость со жгучим вяжущим вкусом, хорошо растворимая в воде. В химическом отношении пероксид водорода очень интересное соединение. Характерна его малая устойчивость: при стоянии медленно разлагается на воду и кислород.
Свет, нагревание, присутствие щелочей, соприкосновение с окислителями или восстановителями ускоряют процесс разложения. Степень окисления кислорода в пероксиде водорода = - 1, т.е. имеет промежуточное значение между степенью окисления кислорода в воде (-2) и в молекулярном кислороде (0), поэтому пероксид водорода проявляет окислительно-восстановительную двойственность. Окислительные свойства пероксида водорода выражены гораздо сильнее, чем восстановительные, и проявляются они в кислой, щелочной и нейтральной средах.
-
Применение в медицине и народном хозяйстве.
В медицинских и косметологических целях для обогащения организма кислородом применяют концентратор кислорода - прибор, предназначенный для проведения кислородотерапии:
-
- в реанимационных отделениях больниц и клиник в качестве источника чистого кислорода для оказания помощи больным бронхиальной астмой, хроническим обструктивным бронхитом, сердечно-сосудистыми заболеваниями, интоксикациях, удушьях при травмах, шоковых состояниях и нарушениях деятельности почек.
-
- в стационаре и на дому для лечения больных, страдающих бронхолегочными и иными заболеваниями, которым жизненно необходим чистый воздух.
-
- в санаториях, детских учреждениях, поликлиниках, в спортклубах, на дому и в стационаре для профилактики заболеваний, укрепления иммунитета и приготовления кислородных коктейлей.
Применение кислорода в народном хозяйстве:
-
В авиации применяют для дыхания (кислородные маски), для горения топлива (жидкий кислород).
-
В металлургии - для резки металлов и сварки металлов
-
На взрывных работах (пропитывают пористые материалы)
-
В химическом производстве (для получения кислот)
-
Какие из указанных веществ имеют металлическую связь: Zn; S; C; KH; Al(OH)3; Ca; H2SO4; O2; Ba; H2O .
металлическую связь имеют: Zn, Ca, Ba
Билет №4
-
Азот, его важнейшие соединения. Биологическая роль азота. Применение в медицине и народном хозяйстве.
Азот расположен в главной подгруппе V группы и во втором периоде периодической системы химических элементов Менделеева. Электронная конфигурация азота в основном состоянии:
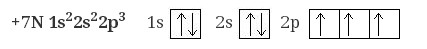
Атом азота содержит на внешнем энергетическом уровне 3 неспаренных электрона и одну неподеленную электронную пару в основном энергетическом состоянии. Следовательно, атом азота может образовать 3 связи по обменному механизму и 1 связь по донорно-акцепторному механизму. Таким образом, максимальная валентность азота в соединениях равна IV. Также характерная валентность азота в соединениях - III.
Степени окисления атома азота – от -3 до +5. Характерные степени окисления азота -3, 0, +1, +2, +3, +4, +5.
Азот в природе существует в виде простого вещества газа N2. Нет цвета, запаха и вкуса. Молекула N2 неполярная, следовательно, в воде азот практически нерастворим.
Азот – это основной компонент воздуха(79% по массе). В земной коре азот встречается в основном в виде нитратов. Входит в состав белков, аминокислот и нуклеиновых кислотв живых организмах.
Типичные соединения азота:
о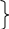 ксид азота (валентность V) N2O5
ксид азота (валентность V) N2O5
азотная кислота HNO3 степень окисления +5
нитраты KNO3, AgNO3
оксид азота (валентность IV) NO2 степень окисления +4
о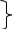 ксид азота (валентность III) N2O3
ксид азота (валентность III) N2O3
азотистая кислота HNO2 степень окисления +3
нитриты NaNO2, Ca(NO2)2
оксид азота (валентность II) NO степень окисления +2
оксид азота (валентность I) N2O степень окисления +1
а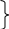 ммиак NH3
ммиак NH3
нитриды металлов Na3N, Ca3N2 степень окисления -3
бинарные соединения азота с неметаллами
Способы получения азота
1. Азот в лаборатории получают при взаимодействии насыщенных растворов хлорида аммония и нитрита натрия. Образующийся в результате реакции обмена нитрит аммония легко разлагается с образованием азота и воды. В колбу наливают раствор хлорида аммония, а капельную воронку раствор нитрита натрия. При приливании нитрита натрия в колбу начинается выделение азота. Собирают выделяющийся азот в цилиндр. Горящая лучинка в атмосфере азота гаснет.
NaNO2 + NH4Cl → NH4NO2 + NaCl
NH4NO2 → N2 + 2H2O
Суммарное уравнение процесса:
NaNO2 + NH4Cl → N2 + NaCl + 2H2O
Азот также образуется при горении аммиака:
4NH3 + 3O2 → 2N2 + 6H2O
2. Наиболее чистый азот получают разложением азидовщелочныхметаллов.
Например, разложением азида натрия:
2NaN3 → 2Na + 3N2
3. Еще один лабораторный способ получения азота — восстановление оксида меди (II) аммиаком при температуре
700 °C:
Биологическая роль кальция. Кальций является одним из основных минералов в организме человека. Он принимает участие во многих биологических процессах. Макроэлемент необходим для формирования костной ткани и зубов, биологического синтеза гормонов, регуляции сосудистого тонуса деятельности сердечно - сосудистой системы. Он также необходим для реализации процесса свертываемости крови при повреждениях.
Применение соединений магния и кальция в медицине:
Жженая магнезия MgO применяется при повышенной кислотности желудочного сока, изжоге, отравлении кислотами. Входит в состав зубных порошков.
Горькая или английская соль MgSO4 × 7 H2O при приеме внутрь служит надежным и быстродействующим слабительным, а при внутримышечных или внутривенных вливаниях снимает судорожное состояние, уменьшает спазмы сосудов.
Как желчегонное его вводят в 12-перстную кишку.
CaCl2 × 6H2O хлорид кальция широко применяется в медицине как кровоостанавливающее средство при легочных, желудочных, кишечных и других кровотечениях, в хирургической практике для повышения свертываемости крови, при аллергических заболеваниях для снятия зуда и в качестве противоядия при отравлении солями магния.
Гипс CaSO4 × 0,5H2O в медицине находит применение для изготовления фиксирующих гипсовых повязок, а также в стоматологической практике для снятия слепков с челюстей при изготовлении искусственных зубов.
Кальций входит в состав препаратов для профилактики остеопороза, в витаминные комплексы для беременных и пожилых.
Применение магния и кальция в народном хозяйстве:
Соли магния и кальция вносят в почвы для химической мелиорации. Целями химической мелиорации являются устранение избыточной кислотности почв, вредной для многих сельскохозяйственных культур (известкование), и устранение избыточной щелочности почв (гипсование).
Соединения магния и кальция в строительстве. Соединения кальция и магния широко используют в строительстве в качестве конструкционных (известняк), отделочных (мрамор) и вяжущих материалов (цемент, известь, гипс).
Кальций широко применяется в металлотермии при получении редкоземельных элементов.
Кальциевые гранулы используются для удаления следов воздуха из электровакуумных приборов.
Сплавы кальция со свинцом находят применение в аккумуляторных батареях и подшипниковых сплавах.
Магний применяется для металлотермического получения некоторых тугоплавких металлов (титана, циркония).
Магний используется для получения легких сплавов (самолетостроение, производство автомобилей), для изготовления осветительных и зажигательных ракет.
Какие из указанных веществ имеют металлическую связь: Zn, S, C, KH, FeCl3, K, Ag, NaCl.
Галогены, биологическая роль и их применение в медицине.
-
препараты, содержащие элементарный (свободный) йод - раствор йода спиртовой, раствор Люголя; -
препараты, способные освобождать элементарный йод - йодинол, йодофор, кальцийодин; -
препараты, диссоциирующие с образованием ионов йода (йодиды) - калия йодид и натрия йодид; -
препараты, содержащие прочно связанный йод - йодолипол, билитраст и другие рентгеноконтрастные вещества; -
радиоактивные препараты йода.
К солям относятся следующие соединения: KCl, CaS, LiHSO4, CuOH, NaOH, Al(OH)3, H[AuCl4], Na3[AlF6], H2[ZnCl4], CaO, MgO, ZnO. Назовите их.
Общая характеристика халькогенов. Характеристика кислорода. Соединения кислорода с водородом. Применение в медицине и народном хозяйстве.
Халькогены — это элементы VIA группы. Родоначальником этой группы является кислород. Кроме кислорода O в эту группу входят S, Se, Te, Po. Название халькогены означает «рождающие руды».
Кислород — самый распространенный элемент на Земле. Он входит в состав воды, которая покрывает поверхность земного шара, образуя его водную оболочку — гидросферу. Кислород входит в состав атмосферы, где на его долю приходится 21%. Кроме этого, он ещё входит в состав многих органических соединений.
Разложение некоторых кислородосодержащих веществ:
летучие водородные соединения (сероводород, аммиак, метан, силан гидриды). При этом также образуются оксиды:
прочие бинарные соединения неметаллов — как правило, соединения серы, углерода, фосфора (сероуглерод, сульфид фосфора и др.):
некоторые оксиды элементов в промежуточных степенях окисления (оксид углерода (II), оксид железа (II) и др.):
Соединения кислорода с водородом. Кислород образует с водородом два соединения: оксид водорода – воду (Н2О) 2Н2 + О2 → 2Н2О
Применение в медицине и народном хозяйстве.
- в реанимационных отделениях больниц и клиник в качестве источника чистого кислорода для оказания помощи больным бронхиальной астмой, хроническим обструктивным бронхитом, сердечно-сосудистыми заболеваниями, интоксикациях, удушьях при травмах, шоковых состояниях и нарушениях деятельности почек.
- в стационаре и на дому для лечения больных, страдающих бронхолегочными и иными заболеваниями, которым жизненно необходим чистый воздух.
- в санаториях, детских учреждениях, поликлиниках, в спортклубах, на дому и в стационаре для профилактики заболеваний, укрепления иммунитета и приготовления кислородных коктейлей.
В авиации применяют для дыхания (кислородные маски), для горения топлива (жидкий кислород).
В металлургии - для резки металлов и сварки металлов
На взрывных работах (пропитывают пористые материалы)
В химическом производстве (для получения кислот)
Какие из указанных веществ имеют металлическую связь: Zn; S; C; KH; Al(OH)3; Ca; H2SO4; O2; Ba; H2O .
Азот, его важнейшие соединения. Биологическая роль азота. Применение в медицине и народном хозяйстве.
3CuO + 2NH3 → 3Cu + N2 + 3H2O
В промышленности азот получают, буквально, из воздуха. При промышленном производстве очень важно, чтобы сырье было дешевым и доступным. Воздуха много и он пока бесплатный.
Используются различные способы выделения азота из воздуха — адсорбционная технология, мембранная и криогенная технологии.
Адсорбционные методыразделения воздуха на компоненты основаны на разделения газовых сред в азотных установках лежит явление связывания твёрдым веществом, называемым адсорбентом, отдельных компонентов газовой смеси.
Основным принципом работы мембранных систем является разница в скорости проникновения компонентов газа через вещество мембраны. Движущей силой разделения газов является разница парциальных давлений на различных сторонах мембраны.
В основе работы криогенных установок разделения воздуха лежит метод разде-ления газовых смеси, основанный на разности температур кипения компонентов воздуха и различии составов находящихся в равновесии жидких и паровых смесей.
Химические свойства азота
При нормальных условиях азот химически малоактивен.
1. Азот проявляет свойства окислителя (с элементами, которые расположены ниже и левее в Периодической системе) и свойства восстановителя (с элементами, расположенными выше и правее). Поэтому азот реагирует с металлами и неметаллами.
1.1. Молекулярный азот при обычных условиях с кислородом не реагирует. Реагирует с кислородом только при высокой температуре (2000оС), на электрической дуге (в природе – во время грозы):
N2 + O2 ⇄ 2NO – Q
Процесс эндотермический, т.е. протекает с поглощением теплоты.
1.2. При сильном нагревании (3000оС - 5000оС или действие электрического разряда) образуется атомарный азот, который реагирует с серой, фосфором, мышьяком, углеродом с образованием бинарных соединений:
2С + N2 → N≡C–C≡N
Молекулярный азот, таким образом, не реагирует с серой, фосфором, мышьяком, углеродом.
1.3. Азот взаимодействует сводородом