Файл: Билеты по общей и неорганической химии для студентов 125Ф3 озо (20222023учебный год) Билет 1.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 07.11.2023
Просмотров: 307
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
й одная кислота (HIO4) степень окисления +7
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
-
Реакция образования нитрида трийода:
3I2 + 5NH3 → 3NH4I + NH3⋅ NI3↓
Нитрид трийода в сухом кристаллическом состоянии разлагается с выделением фиолето-вых паров йода, что демонстрируется как эффектная химическая реакция.
-
Йодиды щелочных металлов очень склонны в растворах присоединять (растворять) молекулы галогенов с образованием полийодидов (перйодидов) — трийодид калия, дихлоройодат I калия:
KI + I2 → KI3
Биологическая роль йода.
Основная биологическая роль йода заключается в синтезе гормонов щитовидной железы (тироксина и трийодтиронина), через которые он и реализует следующие эффекты:
-
стимулирует рост и развитие организма -
регулирует рост и дифференцировку тканей -
повышает артериальное давление, а также частоту и силу сердечных сокращений -
регулирует (увеличивает) скорость протекания многих биохимических реакций -
регулирует обмен энергии, повышает температуру тела -
регулирует белковый, жировой, водно-электролитный обмен -
регулирует обмен витаминов -
повышает потребление тканями кислорода
Применение йода и его соединений в медицине и народном хозяйстве.
В медицине
-
- 5 % спиртовой раствор йода используется в качестве антисептического и кровеостанавливающего средства, однако обрабатывать йодной настойкой можно только небольшие раны, так как йод может вызвать омертвение ткани, что при больших ранах увеличит сроки их заживления. -
В рентгенологических и томографических исследованиях применяются йодсодержащие контрастные препараты
В технике
-
Галогенная лампа - лампа накаливания, в баллон которой добавлены пары галогенов (брома или йода) -
Лазерный термоядерный синтез иодорганические соединения применяются для производства сверхмощных газовых лазеров на возбужденных атомах -
для получения высокочистого титана (Ti), циркония (Zr), гафния (Hf), ниобия (Nb) и других металлов (так называемое йодидное рафинирование металлов); -
применяют в пищевых добавках; -
в фотоделе; -
в аналитической химии - йодометрии;
-
К кислотам относятся следующие соединения: KCl CaS LiHSO4 H2SO4 NaOH Al(OH)3 HCl Na3[AlF6] H3PO4 CaO Mg(OH) HNO3. Назовите их.
Кислоты — сложные вещества, в молекулах которых содержатся атомы водорода, способные замещаться атомами металлов, и кислотные остатки.
H2SO4 – серная кислота
HCl – хлороводород, соляная кислота, хлорид водорода
H3PO4 – ортофосфорная кислота
HNO3 – азотная кислота, селитряная кислота, крепкая водка
Билет №7
-
Соединения углерода. Биологическая роль углерода. Применение в медицине и народном хозяйстве углерода и его соединений.
Углерод расположен в главной подгруппе IV группы и во втором периоде периодической системы химических элементов Менделеева. В природе углерод встречается как в виде простых веществ (алмаз, графит), так и в виде сложных соединений (органические вещества — нефть, природные газ, каменный уголь, карбонаты).
Электронная конфигурация углерода в основном состоянии:
+6С 1s22s22p2 1s
Электронная конфигурация углерода в возбужденном состоянии:
+6С* 1s22s12p3 1s
Атом углерода содержит на внешнем энергетическом уровне 2 неспаренных электрона и 1 неподеленную электронную пару в основном энергетическом состоянии и 4 неспаренных электрона в возбужденном энергетическом состоянии.
Степени окисления атома углерода — от -4 до +4. Характерные степени окисления -4, 0, +2, +4.
Типичные соединения углерода.
о
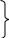 ксид углерода (валентность IV) CO2
ксид углерода (валентность IV) CO2угольная кислота H2CO3 степень окисления +4
карбонаты Cu2CO3, Na2CO3
гидрокарбонаты NaHCO3, Ca(HCO3)2
о
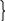 ксид углерода (валентность II) СО степень окисления +2
ксид углерода (валентность II) СО степень окисления +2 муравьиная кислота HCOOH
м
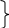 етан CH4
етан CH4карбиды металлов (карбид алюминия Al4C3) степень окисления -4
бинарные соединения с неметаллами (карбид кремния SiC)
Аллотропия углерода.
Углерод в природе существует в виде нескольких аллотропных модификаций: алмаз, графит, карбин, фуллерен.
Алмаз — это модификация углерода с атомной кристаллической решеткой. Алмаз — самое твердое минеральное кристаллическое вещество, прозрачное, плохо проводит электрический ток и тепло. Атомы углерода в алмазе находятся в состоянии sp3-гибридизации.
Графит — это аллотропная модификация, в которой атомы углерода находятся в состоянии sp2-гибридизации. При этом атомы связаны в плоские слои, состоящие из шестиугольников, как пчелиные соты. Слои удерживаются между собой слабыми связями. Это наиболее устойчивая при нормальных условиях аллотропная модификация углерода. Графит — мягкое вещество серо-стального цвета, с металлическим блеском. Хорошо проводит электрический ток. Жирный на ощупь.
Карбин — вещество, в составе которого атомы углерода находятся в sp-гибридизации. Состоит из цепочек и циклов, в которых атомы углерода соединены двойными и тройными связями. Карбин — мелкокристаллический порошок серого цвета.
Фуллерен — это искусственно полученная модифицикация углерода. Молекулы фуллерена — выпуклые многогранники С60, С70 и др. Многогранники образованы пяти- и шестиугольниками, в вершинах которых расположены атомы углерода. Фуллерены — черные вещества с металлическим блеском, обладающие свойствами полупроводников.
При нормальных условиях углерод существует, как правило, в виде атомных кристаллов (алмаз, графит), поэтому химическая активность углерода — невысокая.
Качественные реакции:
Качественная реакция на карбонат-ионы CO32- — взаимодействие солей-карбона-тов с сильными кислотами. Более сильные кислоты вытесняют угольную кислоту из солей. При этом выделяется бесцветный газ, не поддерживающий горение –углекислый газ.
Например, карбонат кальциярастворяется в соляной кислоте:
CaCO3 + 2HCl → CaCl2 + H2O + CO2
Качественная реакция на углекислый газ CO2 – помутнение известковой воды при пропускании через нее углекислого газа:
CO2 + Ca(OH)2 → CaCO3 + H2O
При дальнейшем пропускании углекислого газа осадок растворяется, т.к. карбонат кальция под действием избытка углекислого газа переходит в растворимый гидрокарбонат кальция:
CaCO3 + CO2 + H2O → Ca(HCO3)2
Химические свойства углерода
1. Углерод проявляет свойства окислителя (с элементами, которые расположены ниже и левее в Периодической системе) и свойства восстановителя (с элементами, расположенными выше и правее). Поэтому углерод реагирует и с металлами, и с неметаллами.
1.1. Из галогенов углерод при комнатной температуре реагирует с фторомс образованием фторида углерода:
C + 2F2 → CF4
1.2. При сильном нагревании углерод реагирует с серой и кремнием с образованием бинарного соединения сероуглеродаикарбида кремниясоответственно:
C + 2S → CS2
C + Si → SiC
1.3. Углерод не взаимодействует сфосфором.
При взаимодействии углерода с водородом образуется метан. Реакция идет в присутствии катализатора (никель) и при нагревании:
С + 2Н2 → СН4
1.4. С азотом углерод реагирует при действии электрического разряда, образуя
дициан:
2С + N2 → N≡C–C≡N
1.5. В реакциях с активными металлами углерод проявляет свойства окислителя. При этом образуются карбиды:
4C + 3Al → Al4C3
2C + Ca → CaC2
1.6. При нагревании с избытком воздуха графит горит, образуя оксид углерода (IV):
C + O2 → CO2
при недостатке кислорода образуется угарный газ СО:
2C + O2 → 2CO
2. Углерод взаимодействует со сложными веществами:
2.1. Раскаленный уголь взаимодействует с водяным паром с образованием угарного газа и водорода:
C0 + H2+O → C+2O + H20
2.2. Углерод восстанавливает многие металлы из основных и амфотерныхоксидов. При этом образуются металл и угарный газ. Получение металлов из оксидов с помощью углерода и его соединений называют пирометаллургией.
Например, углерод взаимодействует с оксидом цинка с образованием металлического цинка и угарного газа:
ZnO + C → Zn + CO
Также углерод восстанавливает железо из железной окалины:
4С + Fe3O4 → 3Fe + 4CO
При взаимодействии с оксидами активных металлов углерод образует карбиды.
Например, углерод взаимодействует с оксидом кальция с образованием карбида кальция и угарного газа. Таким образом, углерод диспропорционирует (является т окислителем и восстановителем) в данной реакции:
3С + СаО → СаС2 + СО
9С + 2Al2O3 → Al4C3 + 6CO
2.3. Концентрированная серная кислота окисляет углерод при нагревании. При этом образуются оксид серы (IV), оксид углерода (IV)и вода:
C + 2H2SO4(конц) → CO2 + 2SO2 + 2H2O
2.4. Концентрированная азотная кислотой