Файл: Билеты по общей и неорганической химии для студентов 125Ф3 озо (20222023учебный год) Билет 1.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 07.11.2023
Просмотров: 304
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
й одная кислота (HIO4) степень окисления +7
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
Фосфор образует различные простые вещества (аллотропные модификации).
Белый фосфор — это вещество состава P4. Мягкий, бесцветный, ядовитый, имеет характерный чесночный запах. Молекулярная кристаллическая решетка, а следовательно, невысокая температура плавления (44°С), высокая летучесть. Очень реакционно способен, самовоспламеняется на воздухе.
Красный фосфор – это модификация с атомной кристаллической решеткой. Формула красного фосфора Pn, это полимер со сложной структурой. Твердое вещество без запаха, красно-бурого цвета, не ядовитое. Это гораздо более устойчивая модификация, чем белый фосфор. В темноте не светится. Образуется из белого фосфора при t=250 - 300оС без доступа воздуха.
Черный фосфор – наиболее стабильная термодинамически и химически наименее активная форма элементарного фосфора. Чёрный фосфор — это чёрное вещество с металлическим блеском, жирное на ощупь и весьма похожее на графит, полностью нерастворимое в воде или органических растворителях.
Известны также такие модификации, как желтый фосфор и металлический фосфор. Желтый фосфор – это неочищенный белый фосфор. При очень высоком давлении фосфор переходит в новую модификацию – металлический фосфор, который очень хорошо проводит электрический ток.

Биологическая роль фосфора.
-
фосфор входит в состав многих веществ организма (фосфолипиды, фосфопротеиды, нуклеотиды, коферменты, ферменты и пр.); -
фосфолипиды являются основным компонентом мембран всех клеток в организме человека; -
в костях фосфор находится в виде гидроксилапатита, в зубах в виде фторапатит, выполняя структурную функцию; -
остатки фосфорной кислоты входят в состав нуклеиновых кислот и нуклеотидов, а также в состав аденозинтрифосфорной кислоты (АТФ) и креатинфосфата – важнейшие аккумуляторы и переносчики энергии; -
остатки фосфорной кислоты входят в состав буферной системы крови, регулируя ее значение рН.
Применение в медицине и народном хозяйстве.
Применение Р с лечебной целью целесообразно в следующих случаях:
-
Заболевания костно-мышечной системы – остеопороз, гетерогенные оссификации, опухолевый остеолиз, частые переломы; -
Гипофосфатемия – недостаток фосфора в организме; -
Оксалатный тип почечнокаменной болезни; -
Гиперкальциемия (переизбыток в организме кальция) при онкологических болезнях.
В качестве препаратов фосфора чаще всего применяют биофосфонаты («Этидронат»), «Кальция глицерофосфат».
Фосфор в фармакалогии
Терапевтическое применение препаратов фосфора основано на том, что в малых дозах они усиливают рост и развитие костной ткани (в растущем организме), стимулируют кроветворение, обладают способностью тормозить окислительные процессы в организме и принимают участие в обмене веществ нервной и мышечной ткани.
Фосфор в народном хозяйстве
Более половины объема мирового производства фосфора перерабатывается в соединения, используемые в синтетических моющих средствах.
Соединения фосфора используют для получения антикоррозионных добавок к маслам и горючему для автомобилей.
Сульфиды фосфора стали необходимы в сражении с ржавчиной в металлургии.
Фосфор используется при производстве спичек.
Из фосфора получают фосфорную кислоту, которая идет на производство удобрений.
-
К оксидам относятся следующие соединения: KCl, CaS, CaO, LiHSO4, CuOH, NaOH, Al(OH)3, H[AuCl4], ZnO, Na3[AlF6], H2[ZnCl4], MgO. Назовите их.
Оксиды - это сложные вещества, состоящие из двух элементов, один из которых кислород со степенью окисления -2.
CaO – оксид кальция, негашеная известь
ZnO – оксид цинка, белила цинковые
MgO – оксид магния
Билет №6
-
Общая характеристика галогенов. Йод и его соединения. Биологическая роль. Применение йода и его соединений в медицине и народном хозяйстве.
Галогены расположены в главной подгруппе VII группы периодической системы химических элементов Менделеева. Электронная конфигурация галогенов в основном состоянии соответствует формуле ns2np5
. Например, электронная конфигурация фтора:
Атомы галогеновсодержат на внешнем энергетическом уровне 1 неспаренный электрон и три неподеленные электронные пары в основном энергетическом состоянии. Следовательно, в основном состоянии атомы галогенов могут образовывать 1 связи по обменному механизму.
При этом у фтора возбужденного состояния нет, т.е. максимальная валентность фтора в соединения равна I.
Однако, в отличие от фтора, за счет вакантной d-орбитали атомы хлора, брома и йода могут переходить в возбужденное энергетическое состояние.
Таким образом, максимальная валентность галогенов (кроме фтора) в соединениях равна VII. Также для галогенов характерны валентностиI, III,V.
Степени окисления атома галогенов – от -1 до +7. Характерные степени окисления -1, 0, +1, +3, +5, +7. Для фтора характерная степень окисления -1 и валентность I.
Галогены образуют двухатомные молекулы например: I2, Cl2, Br2. В твёрдом состоянии имеют молекулярную кристаллическую решетку. Плохо растворимы в воде, все имеют запах, летучи.
В природе галогены встречаются в виде соединений, в основном, в виде галогенидов.
Йод и его соединения.
Йод является самым тяжёлым из часто встречающихся галогенов и находится в главной подгруппе VII периодической системы Менделеева. Он существует в виде блестящего пурпурно-чёрного неметаллического твёрдого вещества в стандартных условиях, которое плавится с образованием глубокой фиолетовой жидкости. Электронная конфигурация йода в основном состоянии:
+17 I 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p5
Атом йодасодержит на внешнем энергетическом уровне 1 неспаренный электрон и 3 неподеленных электронных пары
в основном энергетическом состоянии. Следовательно, атом йода может образовывать 1 связь по обменному механизму. За счет вакантной d-орбитали атомы йода могут переходить в возбужденное энергетическое состояние:
+17 I 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p4 5d1
+17 I 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p3 5d2
+17 I 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s1 5p3 5d3
Для атома йода в возбужденном энергетическом состоянии характерна валентность VII.
Степени окисления атома йода – от -1 до +7. Характерные степени окисления -3, 0, +1, +3, +5.
Типичные соединения йода:
й одоводород, йодоводородная кислота (HI) степень окисления -1
одоводород, йодоводородная кислота (HI) степень окисления -1
cоли йодноватой кислоты - йодаты NaI
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
одноватая кислота (HIO3) степень окисления +5
оксиды йода, пентаоксид (пятиокись) йода (I2O5)
й одная кислота (HIO4) степень окисления +7
одная кислота (HIO4) степень окисления +7
соли йодной кислоты - периодаты NaIO4
Способы получения йода
Получение йода осуществляют путем окисления ионов I- сильными окислителями:
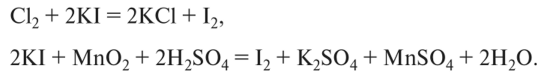
Химические свойства йода
Химически йод довольно активен, хотя и в меньшей степени, чем хлор и бром.
-
Довольно известной качественной реакцией на йод является его взаимодействие с крахмалом, при котором наблюдается синее окрашивание в результате образования соединения включения. Эту реакцию открыли в 1814 году Жан-Жак Колен (Jean-Jacques Colin) и Анри-Франсуа Готье де Клобри (Henri-François Gaultier de Claubry). -
С металлами йод при легком нагревании энергично взаимодействует, образуя йодиды:
Hg + I2 → HgI2
-
С водородом йод реагирует только при нагревании и не полностью, образуя йодоводород:
H2 + I2 → 2HI
-
Йод является окислителем, менее сильным, чем фтор, хлор и бром. Сероводород H2S, Na2S2O3 и другие восстановители восстанавливают его до иона I−:
I2 + H2S → S + 2HI
I2 + 2Na2S2O3 → 2NaI + Na2S4O6
Последняя реакция также используется в аналитической химии для определения йода.