Файл: Билеты по общей и неорганической химии для студентов 125Ф3 озо (20222023учебный год) Билет 1.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 07.11.2023
Просмотров: 305
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
й одная кислота (HIO4) степень окисления +7
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
Физические свойства
Щелочные металлы имеют серебристо-белый цвет с металлическим блеском. Цезий – серебристо-жёлтый металл. Это наиболее активные и мягкие металлы. Натрий, калий, рубидий, цезий режутся ножом. По мягкости напоминают воск.
Щелочноземельные металлы имеют серый цвет. По сравнению со щелочными металлами являются более твёрдыми, плотными веществами. Ножом можно разрезать только стронций. Самый плотный металл – радий (5,5 г/см3).
Наиболее лёгкими металлами являются литий, натрий и калий. Они плавают на поверхности воды.
Химические свойства
Щелочные и щелочноземельные металлы реагируют с простыми веществами и сложными соединениями, образуя соли, оксиды, щёлочи. Основные свойства активных металлов описаны в таблице.
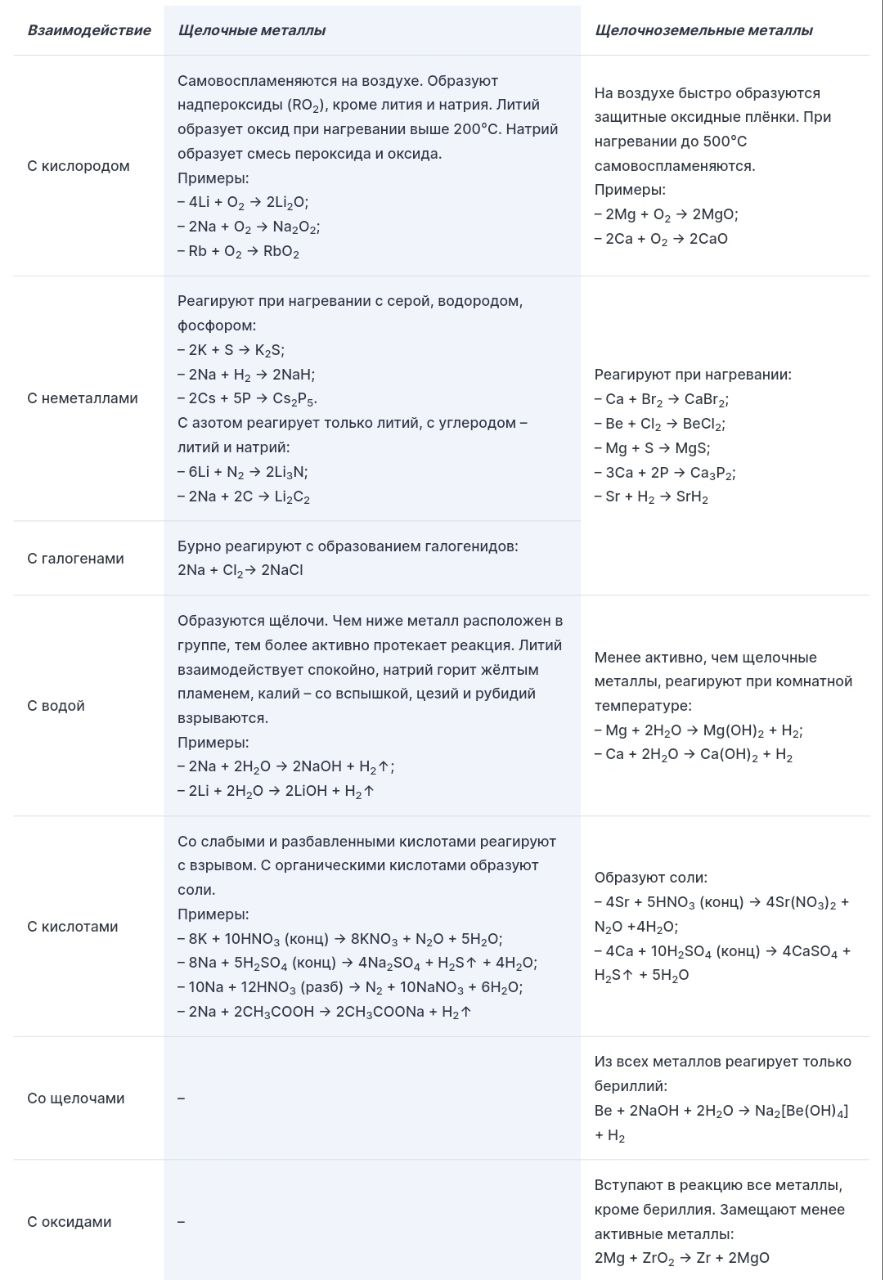
Качественные реакции
Щелочные и щелочноземельные металлы можно обнаружить с помощью качественной реакции. При горении металлы окрашиваются в определённый цвет. Например, натрий горит жёлтым пламенем, калий – фиолетовым, барий – светло-зелёным, кальций – тёмно-оранжевым.
Роль щелочных металлов в организме человека
Щелочные металлы и их соединения играют важную роль в организме человека.
Натрий широко распространен во всех органах, тканях и биологических жидкостях организма человека. Достаточная концентрация натрия содержится в желудочном соке. Большая же часть натрия находится во внеклеточных жидкостях - около 50%, в костях и хрящах - около 40% и до 10% - внутри клеток. В процессе внутриклеточного и межклеточного обмена натрий играет важную роль. Вместе с калием он участвует в возникновении нервного импульса, занимает важное место в механизме кратковременной памяти, оказывает воздействие на состояние мышечной и сердечно - сосудистой систем; ионы натрия и хлора также играют важную роль в секреции соляной кислоты в желудке. Взаимодействие ионов натрия и калия выполняет два важных взаимосвязанных процесса: во-первых, поддерживает постоянное осмотическое давление, а во-вторых, поддерживает постоянный объем жидкости.
Цезий и рубидий малоизучены. Эти элементы находятся в окружающей среде и поступают в организм в основном с пищей. Установлено их постоянное наличие в организме. Однако до сих пор эти элементы не считаются биотическими. Рубидий и цезий найдены во всех исследованных органах млекопитающих и человека. Поступая в организм с пищей, они быстро всасываются из желудочно-кишечного тракта в кровь. Средний уровень рубидия в крови составляет 2,3-2,7 мг/л, причем его концентрация в эритроцитах почти в три раза выше, чем в плазме. Рубидий и цезий равномерно распределяются в органах и тканях, причем, рубидий, в основном, накапливается в мышцах, а цезий поступает в кишечник и реабсорбируется в нисходящих петлях его отдела. В лаборатории И. П. Павлова Боткин установил: хлориды цезия и рубидия вызывают повышение артериального давления на длительное время, и, что это действие связано, главным образом, с усилением сердечнососудистой деятельности и сужением периферических сосудов. Это открытие стали применять в фармацевтике.
Установлено адреноблокирующее и симпатомиметическое воздействие солей цезия и рубидия на центральные и периферические адренореактивные структуры, которое особенно ярко выражено при подавлении тонуса симпатического отдела центральной нервной системы и дефиците катехоламинов. Солям этих металлов свойственен, главным образом, бетта-адреностимулирующий эффект.
Соли рубидия и цезия воздействуют также на неспецифические показатели иммунобиологической резистентности - они вызывают значительное увеличение титра комплемента, активности лизоцима, фагоцитарной активности лейкоцитов. Есть указание на стимулирующее влияние солей рубидия и цезия на функции кроветворных органов. В микродозах они вызывают стимуляцию эритро- и лейкопоэза (на 20-25%), кроме того, заметно повышают резистентность эритроцитов, увеличивают содержание в них гемоглобина.
Франций является радиоактивным элементом. Его соли использовались для обнаружения раковых опухолей, но по причине чрезвычайно высокой стоимости эту соль в масштабных разработках использовать невыгодно.
Роль щелочноземельных металлов в организме человека
Магний содержится в тканях животных и растений (например, в хлорофилле), является кофактором многих ферментативных реакций, необходим при синтезе АТФ, участвует в передаче нервных импульсов, активно применяется в медицине (бишофитотерапия и др.). Кальций — распространенный макроэлемент в организме растений, животных и человека. В организме человека и других позвоночных большая его часть находится в скелете и зубах. В костях кальций содержится в виде гидроксиапатита. Из различных форм карбоната кальция состоят минеральные «скелеты» некоторых представителей многих групп беспозвоночных (губки, кишечнополостные, моллюски и др.). Ионы кальция участвуют в процессах свертывания крови, а также служат одним из универсальных вторичных посредников внутри клеток и регулируют самые разные внутриклеточные процессы: мышечное сокращение, экзоцитоз, в том числе секрецию гормонов и нейромедиаторов. Стронций может замещать кальций в природных тканях, так как схож с ним по свойствам. В организме человека масса стронция составляет около 1 % от массы кальция.
На данный момент о биологической роли бериллия, бария и радия ничего не известно. Все соединения бария (кроме сульфата ввиду его чрезвычайно малой раствори-мости) и бериллия ядовиты. Радий чрезвычайно радиотоксичен. В организме он ведёт себя подобно кальцию — около 80 % поступившего в организм радия накапливается в костной ткани. Большие концентрации радия вызывают остеопороз, самопроизвольные переломы костей и злокачественные опухоли костей и кроветворной ткани. Опасность представляет также радон — газообразный радиоактивный продукт распада радия.
-
Напишите электронно-графическую формулу электронных оболочек атома азота.
N
+7


2 5
Билет №12
-
Общая характеристика галогенов. Йод и его соединения. Биологическая роль. Применение йода и его соединений в медицине и народном хозяйстве.
Галогены расположены в главной подгруппе VII группы периодической системы химических элементов Менделеева. Электронная конфигурация галогенов в основном состоянии соответствует формуле ns2np5. Например, электронная конфигурация фтора:
Атомы галогеновсодержат на внешнем энергетическом уровне 1 неспаренный электрон и три неподеленные электронные пары в основном энергетическом состоянии. Следовательно, в основном состоянии атомы галогенов могут образовывать 1 связи по обменному механизму.
При этом у фтора возбужденного состояния нет, т.е. максимальная валентность фтора в соединения равна I.
Однако, в отличие от фтора, за счет вакантной d-орбитали атомы хлора, брома и йода могут переходить в возбужденное энергетическое состояние.
Таким образом, максимальная валентность галогенов (кроме фтора) в соединениях равна VII. Также для галогенов характерны валентностиI, III,V.
Степени окисления атома галогенов – от -1 до +7. Характерные степени окисления -1, 0, +1, +3, +5, +7. Для фтора характерная степень окисления -1 и валентность I.
Галогены образуют двухатомные молекулы например: I2, Cl2, Br2. В твёрдом состоянии имеют молекулярную кристаллическую решетку. Плохо растворимы в воде, все имеют запах, летучи.
В природе галогены встречаются в виде соединений, в основном, в виде галогенидов.
Йод и его соединения.
Йод является самым тяжёлым из часто встречающихся галогенов и находится в главной подгруппе VII периодической системы Менделеева. Он существует в виде блестящего пурпурно-чёрного неметаллического твёрдого вещества в стандартных условиях, которое плавится с образованием глубокой фиолетовой жидкости. Электронная конфигурация йода
в основном состоянии:
+17 I 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p5
Атом йодасодержит на внешнем энергетическом уровне 1 неспаренный электрон и 3 неподеленных электронных пары в основном энергетическом состоянии. Следовательно, атом йода может образовывать 1 связь по обменному механизму. За счет вакантной d-орбитали атомы йода могут переходить в возбужденное энергетическое состояние:
+17 I 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p4 5d1
+17 I 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p3 5d2
+17 I 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s1 5p3 5d3
Для атома йода в возбужденном энергетическом состоянии характерна валентность VII.
Степени окисления атома йода – от -1 до +7. Характерные степени окисления -3, 0, +1, +3, +5.
Типичные соединения йода: