Файл: Билеты по общей и неорганической химии для студентов 125Ф3 озо (20222023учебный год) Билет 1.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 07.11.2023
Просмотров: 316
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
й одная кислота (HIO4) степень окисления +7
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
-
Напишите уравнение реакции между серной кислотой и гидроксидом бария.
2HCl + Ba(OH)2 → 2H2O + BaCl2
Билет №17
-
Сера. Важнейшие соединения серы. Действие сероводорода на организм. Применение серы и ее соединений в медицине.
Сера расположена в главной подгруппе VI группы и в третьем периоде периодической системы химических элементов Менделеева.
Электронная конфигурация серыв основном состоянии:
Атом серысодержит на внешнем энергетическом уровне 2 неспаренных электрона и две неподеленные электронные пары в основном энергетическом состоянии. Следовательно, атом серы может образовывать 2 связи по обменному механизму, как и кислород. Однако, в отличие от кислорода, за счет вакантной 3d орбитали атом серы может переходить в возбужденные энергетические состояния.
Электронная конфигурация серы впервом возбужденном состоянии:
Электронная конфигурация серы во втором возбужденном состоянии:
Таким образом, максимальная валентность серы в соединениях равна VI. Также для серы характерна валентность — IV.
Степени окисления атома серы – от -2 до +4. Характерные степени окисления -2, 0, +4, +6.
Сера образует различные простые вещества (аллотропные модификации).
Н
 аиболее устойчивая модификация серы – ромбическая сера S8.Это хрупкое вещество желтого цвета.
аиболее устойчивая модификация серы – ромбическая сера S8.Это хрупкое вещество желтого цвета. 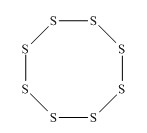
Моноклинная сера – это аллотропная модификация серы, в которой атомы соединены в циклы в виде «короны». Это твердое вещество, состоящее из темно-желтых игл, устойчивое при температуре более 96
оС, а при обычной температуре превращающееся в ромбическую серу.

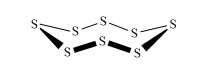
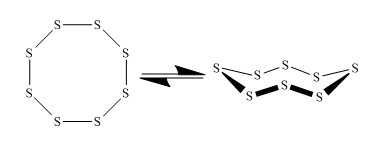
Пластическая сера – это вещество, состоящее из длинных полимерных цепей. Коричневая резиноподобная аморфная масса, нерастворимая в воде.

В природе сера встречается:
-
в самородном виде; -
в составе сульфидов (сульфид цинка ZnS, пирит FeS2, сульфид ртути HgS - киноварь и др.) -
в составе сульфатов (CaSO4·2H2O - гипс, Na2SO4·10H2O - глауберова соль)
Типичные соединения серы
О
 ксид серы(VI) SO3
ксид серы(VI) SO3Серная кислота H2SO4 степень окисления +6
Сульфаты Na2SO4
Галогенангидриды: SО2Cl2
О
 ксид серы (IV) SO2
ксид серы (IV) SO2Сернистая кислота H2SO3
Сульфиты Na2SO3 степень окисления +4
Гидросульфиты Mg(HSO3)2
Галогенангидриды: SOCl2
Сероводород H2S степень окисления -2
Сульфиды металлов FeS
Способы получения серы
1. В промышленных масштабах серу получают открытым способом на месторожде-ниях самородной серы, либо из вулканов. Из серной руды серу получают также пароводяными, фильтрационными, термическими, центрифугальными и экстракцион-ными методами. Пароводяной метод - это выплавление из руды с помощью водяного пара.
2. Способ получения серы в лаборатории – неполное окисление сероводорода.
2H2S + O2 → 2S + 2H2O
3. Еще один способ получения серы –взаимодействие сероводорода с оксидом серы (IV):
2H2S + SO2 → 3S + 2H2O
Химические свойства серы
В нормальных условиях химическая активность серы невелика: при нагревании сера активна, и может быть как окислителем, так и восстановителем.
1. Сера проявляет свойства окислителя (при взаимодействии с элементами, которые расположены ниже и левее в Периодической системе) и свойства восстановителя (с элементами, расположенными выше и правее). Поэтому сера реагирует с металлами и неметаллами.
1.1. При горении серы на воздухе образуется оксид серы (IV):
S + O2 → SO2
1.2. При взаимодействии серы с галогенами (со всеми, кроме йода) образуются галогениды серы:
S + Cl2 → SCl2 (S2Cl2)
S + 3F2 → SF6
1.3. При взаимодействии фосфора и углерода с серой образуются сульфиды фосфора и сероуглерод:
2P + 3S → P2S3
2P + 5S → P2S5
2S + C → CS2
1.4. При взаимодействии с металлами сера проявляет свойства окислителя, продукты реакции называют сульфидами. С щелочными металлами сера реагирует без нагревания, а с остальными металлами (кроме золота и платины) – только при нагревании.
Например, железо и ртуть реагируют с серой с образованием сульфидовжелеза (II) и ртути:
S + Fe → FeS
S + Hg → HgS
Еще пример: алюминийвзаимодействует с серой с образованием сульфида алюминия:
3S + 2Al → Al2S3
1.5. С водородом сера взаимодействует при нагревании с образованием сероводорода:
S + H2 → H2S
2. Со сложными веществами сера реагирует, также проявляя окислительные и восстановительные свойства. Сера диспропорционирует при взаимодействии с некоторыми веществами.
2.1. При взаимодействии с окислителями сера окисляется до оксида серы (IV) или до серной кислоты(если реакция протекает в растворе).
Например, азотная кислота окисляет серу до серной кислоты:
S + 6HNO3 → H2SO4 + 6NO2 + 2H2O
Серная кислота также окисляет серу. Но, поскольку S+6 не может окислить серу же до степени окисления +6, образуется оксид серы (IV):
S + 2H2SO4 → 3SO2 + 2H2O
Соединения хлора, например, бертолетова соль, также окисляют серу до +4:
3S + 2KClO3 → 3SO2 + 2KCl
Взаимодействие серы с сульфитами (при кипячении) приводит к образованию тиосульфатов:
S + Na2SO3 → Na2S2O3
2.2. При растворении в щелочах сера диспропорционирует до сульфита и сульфида.
Например, сера реагирует с гидроксидом натрия:
S + 6NaOH → Na2SO3 + 2Na2S + 3H2O
При взаимодействии с перегретым паром сера диспропорционирует:
3S + 2H2O(пар) → 2H2S + SO2
Качественные реакции:
а) Качественная реакция на сульфит- и сульфат-ионы
Сера образует ряд кислот. Соли серной кислоты H
2SO4 называют сульфатами, сернистой H2SO3 - сульфитами. Качественная реакция на сульфат и сульфит-ионы - реакция с растворимой солью бария.
BaCl2 + Na2SO3 → BaSO3↓ + 2NaCl
BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl
В двух пробирках появляются белые кристаллические осадки сульфата бария и сульфита бария. Как различить эти осадки? При добавлении раствора азотной кислоты осадок сульфита бария растворяется, а осадок сульфата бария остается без изменения.
б) Качественные реакции на сульфид-анион S2-
Из сульфидов растворимы сульфиды только щелочных металлов и аммония. Нерастворимые сульфиды имеют специфическую окраску, по которым можно определить тот или иной сульфид.
Окраска:
MnS - телесный (розовый).
ZnS - белый.
PbS - черный.
Ag2S - черный.
CdS - лимонно-желтый.
SnS - шоколадный.
HgS (метакиноварь) - черный.
HgS (киноварь) - красный.
Sb2S3 - оранжевый.
Bi2S3 - черный.
Некоторые сульфиды при взаимодействии с кислотами - неокислителями образуют токсичный газ сероводород H2S с неприятным запахом (тухлых яиц):
Na2S + 2HBr → 2NaBr + H2S↑
S2- + 2H+ → H2S↑
А некоторые устойчивы к разбавленным растворам HCl, HBr, HI, H2SO4, HCOOH, CH3COOH - к примеру CuS, Cu2S, Ag2S, HgS, PbS, CdS, Sb2S3, SnS и некоторые другие. Но они переводятся в раствор конц. азотной кислотой при кипячении (Sb2S3и HgS растворяются тяжелее всего, причем последний гораздо быстрее растворится в царской водке): to
CuS + 8HNO3 → CuSO4 + 8NO2↑ + 4H2O
Также сульфид-анион можно выявить, приливая раствор сульфида к бромной воде:
S2- + Br2 → S↓ + 2Br-
Образующаяся сера выпадает в осадок.
в) Качественная реакция на тиосульфат-анион S2O3
При добавлении раствора серной или соляной кислоты к раствору тиосульфата образуется диоксид серы SO2 и выпадает в осадок элементарная сера S:
S2O3 + 2H+ → S↓ + SO2↑ + H2O
Действие сероводорода на организм
Сероводород в зависимости от концентрации оказывает как положительное, так и отрицательное действие на жизнедеятельность организма и его физиологические процессы. Это химическое соединение может образовываться во внутренних средах или поступать из внешнего окружения. Влияние сероводорода на организм человека многогранное, как полезное, так и отравляющее, способное вызвать мгновенную смерть.