Файл: Билеты по общей и неорганической химии для студентов 125Ф3 озо (20222023учебный год) Билет 1.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 07.11.2023
Просмотров: 320
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
й одная кислота (HIO4) степень окисления +7
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
Вещество образуется в процессе гниения белковых соединений, которые содержат в своём составе аминокислоты с серой. Сероводород в незначительном количестве вырабатывается в кишечнике человека.
Эндогенный, образующийся в организме, сероводород важен для нормальных физиологических процессов. Он принимает активное участие в синаптической передаче нервных импульсов. Положительно влияет на головной мозг, способствует развитию памяти и восприятию новой информации.
Газ является спазмолитиком, при его использовании расслабляются кровеносные сосуды мелкого калибра и гладкая мускулатура полых органов. Поэтому сероводород – это профилактика развития сердечно-сосудистой патологии.
Вещество регулирует внутриклеточные обменные процессы.
В небольших объёмах действует как антиоксидант, снижает выраженность воспаления тканей.
Сероводород, находящийся в воздухе, опасен для человека (класс опасности-2). Газ попадает внутрь организма ингаляционным и трансдермальным (через кожу) путём.
Внешние источники отравляющего вещества:
-
полигоны твёрдых и жидких отходов, в которых активно проходят процессы гниения; -
выгребные ямы, канализация, очистные водные сооружения, туннели; -
нефтеперерабатывающая, химическая и газовая промышленность; -
предприятия по производству целлюлозы, чугуна, асфальтной крошки; -
химические лаборатории.
Попадая в организм, вещество окисляется и образует неорганические соединения. При вдыхании сероводород парализует обонятельные нервы, и человек перестаёт ощущать запах газа, который оказывает смертельное действие. Это часто приводит к сильным отравлениям из-за неспособности своевременно распознать и прекратить контакт с токсическим источником.
При проникновении во внутренние среды организма механизм токсического действия направлен на поражение нервной и кроветворной системы, костный мозг.
Газ оказывает поражающее воздействие на слизистые оболочки. Из-за разрушения гемоглобина приводит к выраженной гипоксии (кислородное голодание). Такое системное влияние нарушает функциональность всех органов. Первым под токсическое отравление попадает мозг.
Применение серы и ее соединений в медицине.
-
Очищенная мелкодисперсная сера применяется наружно в 15—20%-ных мазях и присыпках при лечении псориаза, себореи, чесотки и внутрь в качестве слабительного и отхаркивающего средства. Она взаимодействует с органическими веществами, образуя сульфиды и пентатионовую кислоту, которые оказывают противомикробное и противопаразитарное действие. -
Радиоактивная сера и меченные ею соединения используются в экспериментальной медицине в качестве индикаторов. -
Если в лаборатории разлили ртуть (возникла опасность отравления ртутными парами!), ее первым делом собирают, а те места, из которых серебристые капли не извлекаются, засыпают порошкообразной серой. Ртуть и сера вступают в реакцию даже в твердом состоянии — при простом соприкосновении. Образуется кирпично-красная киноварь — сульфид ртути — химически крайне инертное и безвредное вещество. -
Сероводородные (H2S) ванны благоприятно влияют на организм при различных заболеваниях. -
Большое распространение получили производные моноамида серной кислоты — сульфаниламидные препараты: стрептоцид, норсульфазол, сульфадиметоксин, сульфамонометоксин, фталазол и др., обладающие антибактериальной активностью. -
Пентагидрат тиосульфата натрия Na2S2O3-5H2O применяется как противоядие при отравлениях цианидами, синильной кислотой, солями тяжелых металлов, йодом. -
Тиосульфат натрия Na2S2O3 в виде 30%-ного раствора применяется как антисептическое средство при аллергических заболеваниях, артритах, невралгиях, красной волчанке. Наружно тиосульфатом лечат чесотку, грибковые заболевания.
При подкислении водных растворов тиосульфата образуются сера и оксид серы (IV):
Эта реакция лежит в основе метода лечения чесотки по Демьяновичу: сначала в кожу втирается раствор Na2S2O3, а затем раствор НС1. Образующиеся при этом продукты реакции (SO2 и S) оказывают противопаразитарное действие.
Na2S2O3 используется при отравлении цианидами, так как окисляет цианид-анион в значительно менее ядовитый тиоцианат-анион:
Со многими ионами-токсикантами: кадмия, меди (I), ртути (II), свинца (II), серебра - тиосульфат-анион образует прочные комплексы и малорастворимые нетоксичные соединения, поэтому он используется как универсальный антидот:
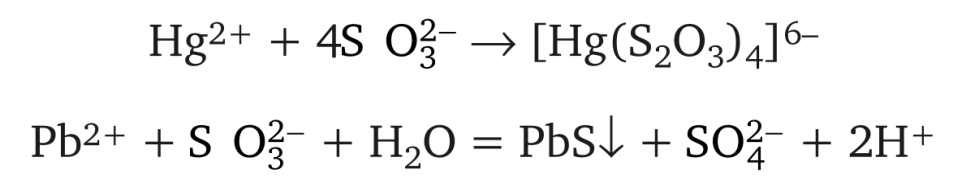
-
Серная кислота H2SO4 применяется как противоядие при отравлениях солями бария и свинца, для подкисления микстур. Определение сульфатов в моче позволяет судить о процессах гниения белков в кишечнике.
Концентрированная серная кислота оказывает прижигающее действие путем дегидратации поверхностных элементов с образованием плотного струпа (коагуляционный некроз).
-
В медицине широкое применение нашли различные сульфаты: Na2SO4-10H2O — глауберова соль, CaSO4-2H2O — гипс, 2CaSO4-H2O — алебастр, MgSO4-7H2O, BaSO4, CuSO4, ZnSO4, FeSO4-7H2O — железный купорос, KA1(SO4)2-12H2O — алюмокалиевые квасцы. -
Сукцимер,
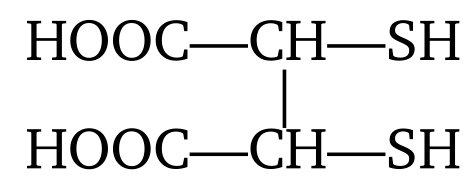
пеницилламин
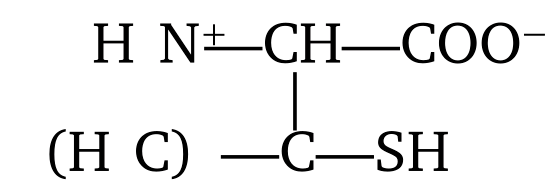
и унитиол
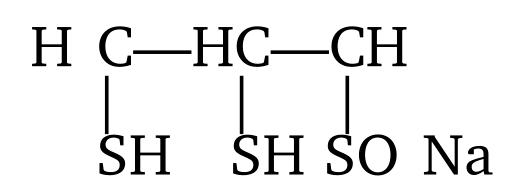
называют антидотами. Они используются при отравлениях мышьяком, ртутью, кадмием, свинцом, хромом, кобальтом и некоторыми радиоактивными элементами, так как являясь мягкими основаниями, связывают мягкие кислоты — ионы токсичных металлов, согласно принципу ЖМКО, в прочные комплексные соединения, которые затем выводятся с мочой из организма
, например:
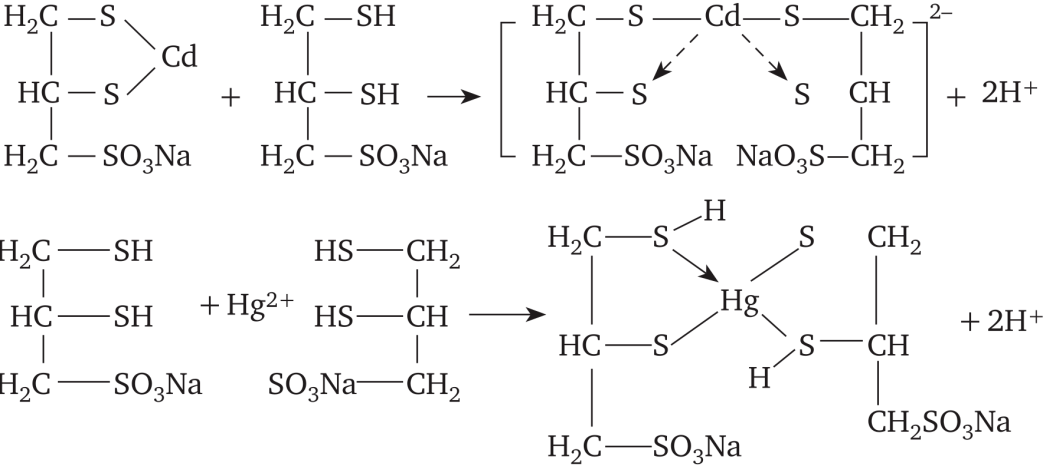
Это интересно!
Издавна использовалась сера в медицине — ее пламенем окуривали больных, ее включали в состав различных мазей для лечения кожных заболеваний. Древние греки использовали серу в военном деле в составе снарядов.
Все сульфамидные препараты — сульфидин, норсульфазол, сульфадимезин, стрептоцид и др. подавляют активность многочисленных микробов. Все эти лекарства — органические соединения серы. Многие антибиотики можно рассматривать как органические производные серы, в частности сера входит в состав пенициллина. Мелкодисперсная элементарная сера — основа мазей, применяемых при лечении заболеваний кожи.
-
Напишите уравнение реакции между фосфорной кислотой и гидроксидом кальция.
2H3PO4 + 3Ca(OH)2 → 6H2O + Ca3(PO4)2
Билет №18
-
Характеристика железа. Биологическая роль железа. Применение железа и его соединений в медицине.
Элемент железо расположен в побочной подгруппе VIII группы и в четвертом периоде периодической системы химических элементов Менделеева.
Электронная конфигурация железав основном состоянии:
+26Fe 1s22s22p63s23p64s23d6
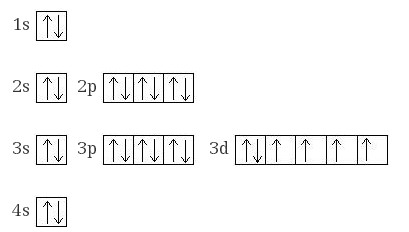
Железопроявляет ярко выраженные магнитные свойства.
Ж
 елезо– металл серебристо-белого цвета, с высокой химической активностью и высокой ковкостью. Обладает высокой тепло- и электропроводностью.
елезо– металл серебристо-белого цвета, с высокой химической активностью и высокой ковкостью. Обладает высокой тепло- и электропроводностью.Температура плавления 1538оС, температура кипения 2861оС.
Ж
 елезодовольно распространено в земной коре (порядка 4% массы земной коры). По распространенности на Земле железо занимает 4-ое место среди всех элементов и 2-ое место среди металлов. Содержание в земной коре — около 8%.
елезодовольно распространено в земной коре (порядка 4% массы земной коры). По распространенности на Земле железо занимает 4-ое место среди всех элементов и 2-ое место среди металлов. Содержание в земной коре — около 8%.В природе железо в основном встречается в виде соединений:
Красный железняк Fe
2O3 (гематит).
Магнитный железняк Fe3O4 или FeO·Fe2O3 (магнетит).

В природе также широко распространены сульфиды железа, например, пирит FeS2.

Встречаются и другие минералы, содержащие железо.
Способы получения
Железов промышленности получают из железной руды, гематита Fe2O3или магнетита (Fe3O4 илиFeO·Fe2O3).
1. Один из основных способов производства железа – доменный процесс. Доменный процесс основан на восстановлении железа из оксида углеродом в доменной печи.
В печь загружают руду, кокс и флюсы.
Шихта – смесь исходных материалов, а в некоторых случаях и топлива в определённой пропорции, которую обрабатывают в печи.
Каменноугольный кокс – это твёрдый пористый продукт серого цвета, получаемый путем коксования каменного угля при температурах 950—1100 °С без доступа воздуха. Содержит 96—98 % углерода.
Флюсы – это неорганические вещества, которые добавляют к руде при выплавке металлов, чтобы снизить температуру плавления и легче отделить металл от пустой породы.
Шлак – расплав (а после затвердевания – стекловидная масса), покрывающий поверхность жидкого металла. Шлак состоит из всплывших продуктов пустой породы с флюсами и предохраняет металл от вредного воздействия газовой среды печи, удаляет примеси.
В печи кокс окисляется до оксида углерода (II):
2C + O2 → 2CO
Затем нагретый угарный газ восстанавливает оксид железа (III):
3CO + Fe2O3 → 3CO2 + 2Fe
Процесс получения железа – многоэтапный и зависит от температуры.
Наверху, где температура обычно находится в диапазоне между 200 °C и 700 °C, протекает следующая реакция:
3Fe2O3 + CO → 2Fe3O4 + CO2
Ниже в печи, при температурах приблизительно 850 °C, протекает восстановление смешанного оксида железа (II, III) до оксида железа (II):
Fe3O4 + CO → 3FeO + CO2
Встречные потоки газов разогревают шихту