Файл: Билеты по общей и неорганической химии для студентов 125Ф3 озо (20222023учебный год) Билет 1.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 07.11.2023
Просмотров: 321
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
й одная кислота (HIO4) степень окисления +7
й одоводород, йодоводородная кислота (HI) степень окисления -1
йодноватистая кислота (HIO) степень окисления +1
й одноватая кислота (HIO3) степень окисления +5
окисляет углерод также при нагревании. При этом образуются оксид азота (IV), оксид углерода (IV)и вода:
C + 4HNO3(конц) → CO2 + 4NO2 + 2H2O
2.5. Углерод проявляет свойства восстановителя и при сплавлении с некоторыми солями, в которых содержатся неметаллы с высокой степенью окисления.
Например, углерод восстанавливает сульфат натриядо сульфида натрия:
4C + Na2SO4 → Na2S + 4CO
Биологическая роль углерода.
Как и другие элементы - органогены, углерод в виде отдельного элемента не обладает биологическим значением, - биологической ролью обладают его соединения.
Применение в медицине и народном хозяйстве углерода и его соединений.
В медицине:
В фармакологии и медицине широко используются различные соединения углерода - производные угольной кислоты и карбоновых кислот, различные гетероциклы, полимеры и другие соединения. Так, карболен (активированный уголь), применяется для абсорбции газов и выведения из организма различных токсинов; графит (в виде мазей) - для лечения кожных заболеваний; радиоактивные изотопы углерода - для научных медицинских исследований.
В народном хозяйстве:
Графит используется в карандашной промышленности, но в смеси с глиной, для уменьшения его мягкости. Также его используют в качестве смазки при особо высоких или низких температурах. Его невероятно высокая температура плавления, даёт возможность делать из него тигли для заливки металлов. Способность графита проводить электрический ток также даёт возможность изготавливать из него высококачественные электроды.
Алмаз, благодаря исключительной твердости, незаменимый абразивный материал. Алмазным напылением обладают шлифовальные насадки бормашин. Помимо этого, ограненные алмазы — бриллианты используются в качестве драгоценных камней в ювелирных украшениях. Благодаря редкости, высоким декоративным качествам и стечению исторических обстоятельств, бриллиант неизменно является самым дорогим драгоценным камнем. Исключительно высокая теплопроводность алмаза (до 2000 Вт/м·К) делает его перспективным материалом для полупроводниковой техники в качестве подложек для процессоров. Но относительно высокая цена (около 50 долларов/грамм) и сложность обработки алмаза ограничивают его применение в этой области.
о ксид азота (валентность V) N2O5
ксид азота (валентность V) N2O5
азотная кислота HNO3 степень окисления +5
нитраты KNO3, AgNO3
оксид азота (валентность IV) NO2 степень окисления +4
о ксид азота (валентность III) N2O3
ксид азота (валентность III) N2O3
азотистая кислота HNO2 степень окисления +3
нитриты NaNO2, Ca(NO2)2
оксид азота (валентность II) NO степень окисления +2
оксид азота (валентность I) N2O степень окисления +1
гидроксиламин NH2OH степень окисления -1
N2H4 степень окисления -2
NH3 степень окисления -3
нитриды AlN, Ca3N2
Билет №8
Кремний расположен в
главной подгруппе IV группы и в третьем периоде периодической системы химических элементов Менделеева. Электронная конфигурация кремния в основном состоянии:
+14Si 1s22s22p63s23p2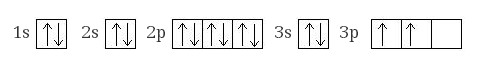
Электронная конфигурация кремния в возбужденном состоянии:
+14Si* 1s22s22p63s13p3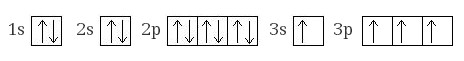
Атом кремния содержит на внешнем энергетическом уровне 2 неспаренных электрона и 1 неподеленную электронную пару в основном энергетическом состоянии и 4 неспаренных электрона в возбужденном энергетическом состоянии.
Степени окисления атома кремния — от -4 до +4. Характерные степени окисления -4, 0, +2, +4.
Кремний — второй по распространенности элемент на Земле после кислорода. Встречается только в виде соединений. Оксид кремния SiO2 образует большое количество природных веществ – горный хрусталь, кварц, кремнезем.
Простое вещество кремний – атомный кристалл темно – серого цвета с металличес-ким блеском, довольно хрупок. Температура плавления 1415 °C, плотность 2,33 г/см3. Полупроводник.
Качественная реакция на силикат - ионы SiO32- — взаимодействие солей-силикатов с сильными кислотами. Кремниевая кислота – слабая. Она легко выделяется из растворов солей кремниевой кислоты при действии на них более сильными кислотами.
Например, если к раствору силиката натрия прилить сильно разбавленный раствор соляной кислоты
, то кремниевая кислота выделится не в виде осадка, а в виде геля. Раствор помутнеет и «застынет».
Na2SiO3 + 2HCl → H2SiO3 + 2NaCl
Типичные соединения кремния
о ксид кремния (валентность IV) SiO2
ксид кремния (валентность IV) SiO2
кремниевая кислота H2SiO3 степень окисления +4
силикаты Na2SiO3
бинарные соединения с неметаллами (карбид кремния SiC)
силан SiH4 степень окисления -4
силициды металлов (силицид натрия Na4Si)
Химические свойства кремния
При нормальных условиях кремний существует в виде атомного кристалла, поэтому химическая активность кремния крайне невысокая.
1. Кремний проявляет свойства окислителя (при взаимодействии с элементами, которые расположены ниже и левее в Периодической системе) и свойства восстановителя (при взаимодействии с элементами, расположенными выше и правее). Поэтому кремний реагирует и с металлами, и с неметаллами.
1.1. При обычных условиях кремний реагирует с фторомс образованием фторида кремния (IV):
Si + 2F2 → SiF4
При нагревании кремний реагирует схлором, бромом, йодом:
Si + 2Cl2 → SiCl4
Si + 2Br2 → SiBr4
1.2. При сильном нагревании (около 2000оС) кремний реагирует с углеродомс образованием бинарного соединения карбида кремния (карборунда):
C + Si → SiC
При температуре выше 600°С взаимодействует с серой:
Si + 2S → SiS2
1.3. Кремний не взаимодействует с водородом.
1.4. С азотом кремний реагирует в очень жестких условиях:
3Si + 2N2 → Si3N4
1.5. В реакциях с активными металлами кремний проявляет свойства окислителя. При этом образуются силициды:
2Ca + Si → Ca2Si
Si + 2Mg → Mg2Si
1.6. При нагревании выше 400°С кремний взаимодействует
C + 4HNO3(конц) → CO2 + 4NO2 + 2H2O
2.5. Углерод проявляет свойства восстановителя и при сплавлении с некоторыми солями, в которых содержатся неметаллы с высокой степенью окисления.
Например, углерод восстанавливает сульфат натриядо сульфида натрия:
4C + Na2SO4 → Na2S + 4CO
Биологическая роль углерода.
Как и другие элементы - органогены, углерод в виде отдельного элемента не обладает биологическим значением, - биологической ролью обладают его соединения.
-
из различных соединений углерода (белки, жиры, углеводы, нуклеотиды, гормоны, амино- и карбоновые кислоты и др.) состоят все ткани организма; -
является структурным компонентом всех органических соединений; -
его соединения участвуют во всех биохимических процессах; -
при окислении соединений углерода образуется необходимая для организма энергия; -
оксид углерода (IV) CO2, образующийся в результате окисления соединений углерода, стимулирует дыхательный центр, регулирует значение рН крови.
Применение в медицине и народном хозяйстве углерода и его соединений.
В медицине:
В фармакологии и медицине широко используются различные соединения углерода - производные угольной кислоты и карбоновых кислот, различные гетероциклы, полимеры и другие соединения. Так, карболен (активированный уголь), применяется для абсорбции газов и выведения из организма различных токсинов; графит (в виде мазей) - для лечения кожных заболеваний; радиоактивные изотопы углерода - для научных медицинских исследований.
В народном хозяйстве:
Графит используется в карандашной промышленности, но в смеси с глиной, для уменьшения его мягкости. Также его используют в качестве смазки при особо высоких или низких температурах. Его невероятно высокая температура плавления, даёт возможность делать из него тигли для заливки металлов. Способность графита проводить электрический ток также даёт возможность изготавливать из него высококачественные электроды.
Алмаз, благодаря исключительной твердости, незаменимый абразивный материал. Алмазным напылением обладают шлифовальные насадки бормашин. Помимо этого, ограненные алмазы — бриллианты используются в качестве драгоценных камней в ювелирных украшениях. Благодаря редкости, высоким декоративным качествам и стечению исторических обстоятельств, бриллиант неизменно является самым дорогим драгоценным камнем. Исключительно высокая теплопроводность алмаза (до 2000 Вт/м·К) делает его перспективным материалом для полупроводниковой техники в качестве подложек для процессоров. Но относительно высокая цена (около 50 долларов/грамм) и сложность обработки алмаза ограничивают его применение в этой области.
-
Составьте химические формулы соединений азота в соответствии с возможными степенями окисления.
о
 ксид азота (валентность V) N2O5
ксид азота (валентность V) N2O5 азотная кислота HNO3 степень окисления +5
нитраты KNO3, AgNO3
оксид азота (валентность IV) NO2 степень окисления +4
о
 ксид азота (валентность III) N2O3
ксид азота (валентность III) N2O3азотистая кислота HNO2 степень окисления +3
нитриты NaNO2, Ca(NO2)2
оксид азота (валентность II) NO степень окисления +2
оксид азота (валентность I) N2O степень окисления +1
гидроксиламин NH2OH степень окисления -1
N2H4 степень окисления -2
NH3 степень окисления -3
нитриды AlN, Ca3N2
Билет №8
-
Кремний. Распространение в природе. Оксид кремния (IV). Кремниевая кислота. Силикаты.
Кремний расположен в
главной подгруппе IV группы и в третьем периоде периодической системы химических элементов Менделеева. Электронная конфигурация кремния в основном состоянии:
+14Si 1s22s22p63s23p2

Электронная конфигурация кремния в возбужденном состоянии:
+14Si* 1s22s22p63s13p3

Атом кремния содержит на внешнем энергетическом уровне 2 неспаренных электрона и 1 неподеленную электронную пару в основном энергетическом состоянии и 4 неспаренных электрона в возбужденном энергетическом состоянии.
Степени окисления атома кремния — от -4 до +4. Характерные степени окисления -4, 0, +2, +4.
Кремний — второй по распространенности элемент на Земле после кислорода. Встречается только в виде соединений. Оксид кремния SiO2 образует большое количество природных веществ – горный хрусталь, кварц, кремнезем.
Простое вещество кремний – атомный кристалл темно – серого цвета с металличес-ким блеском, довольно хрупок. Температура плавления 1415 °C, плотность 2,33 г/см3. Полупроводник.
Качественная реакция на силикат - ионы SiO32- — взаимодействие солей-силикатов с сильными кислотами. Кремниевая кислота – слабая. Она легко выделяется из растворов солей кремниевой кислоты при действии на них более сильными кислотами.
Например, если к раствору силиката натрия прилить сильно разбавленный раствор соляной кислоты
, то кремниевая кислота выделится не в виде осадка, а в виде геля. Раствор помутнеет и «застынет».
Na2SiO3 + 2HCl → H2SiO3 + 2NaCl
Типичные соединения кремния
о
 ксид кремния (валентность IV) SiO2
ксид кремния (валентность IV) SiO2кремниевая кислота H2SiO3 степень окисления +4
силикаты Na2SiO3
бинарные соединения с неметаллами (карбид кремния SiC)
силан SiH4 степень окисления -4
силициды металлов (силицид натрия Na4Si)
Химические свойства кремния
При нормальных условиях кремний существует в виде атомного кристалла, поэтому химическая активность кремния крайне невысокая.
1. Кремний проявляет свойства окислителя (при взаимодействии с элементами, которые расположены ниже и левее в Периодической системе) и свойства восстановителя (при взаимодействии с элементами, расположенными выше и правее). Поэтому кремний реагирует и с металлами, и с неметаллами.
1.1. При обычных условиях кремний реагирует с фторомс образованием фторида кремния (IV):
Si + 2F2 → SiF4
При нагревании кремний реагирует схлором, бромом, йодом:
Si + 2Cl2 → SiCl4
Si + 2Br2 → SiBr4
1.2. При сильном нагревании (около 2000оС) кремний реагирует с углеродомс образованием бинарного соединения карбида кремния (карборунда):
C + Si → SiC
При температуре выше 600°С взаимодействует с серой:
Si + 2S → SiS2
1.3. Кремний не взаимодействует с водородом.
1.4. С азотом кремний реагирует в очень жестких условиях:
3Si + 2N2 → Si3N4
1.5. В реакциях с активными металлами кремний проявляет свойства окислителя. При этом образуются силициды:
2Ca + Si → Ca2Si
Si + 2Mg → Mg2Si
1.6. При нагревании выше 400°С кремний взаимодействует