ВУЗ: Национальный исследовательский томский политехнический университет
Категория: Учебное пособие
Дисциплина: Химия
Добавлен: 09.02.2019
Просмотров: 10353
Скачиваний: 59
96
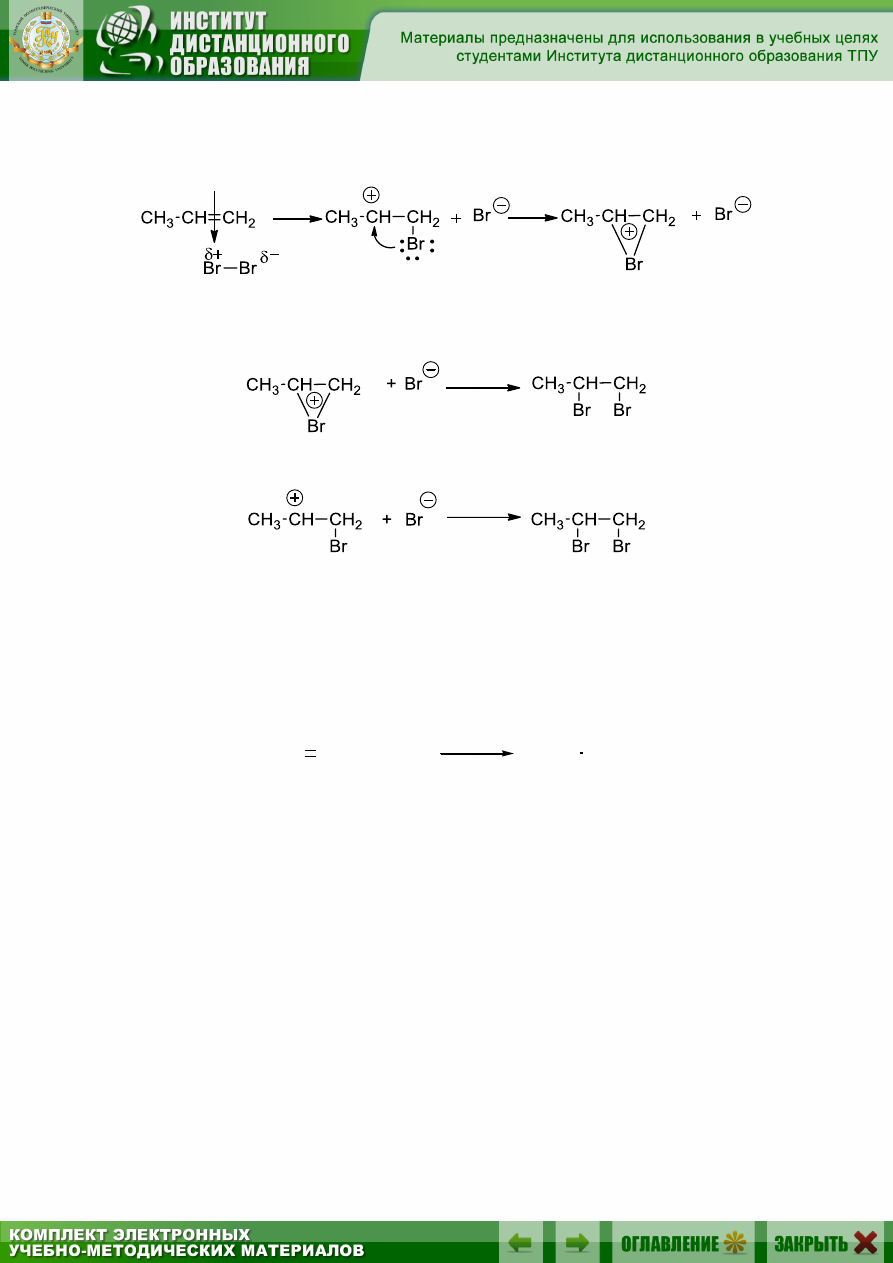
2. От
-комплекса отделяется отрицательный ион брома (Br
–
) и об-
разуется карбокатион ( или ион бромония):
3. Нуклеофил Br
–
атакует циклический ион бромония, или карбо-
катион:
или
Реакция может проходить в темноте, следовательно, в ней не уча-
ствуют свободные радикалы.
6.6.4. Присоединение галогеноводородов
Алкены реагируют с хлористым, бромистым или иодистым водо-
родом с образованием соответствующих алкилгалогенидов:
H
I
CH
3
CH
2
I
CH
2
CH
2
+
этен
иодэтан
Реакцию обычно проводят, пропуская газообразный галогеноводо-
род непосредственно в алкен. Иногда используют растворитель средней
полярности, например уксусную кислоту, которая растворяет и поляр-
ный галогеноводород, и неполярный алкен. Водные растворы галогено-
водородов не применяют, чтобы не происходило присоединения воды
к алкенам.
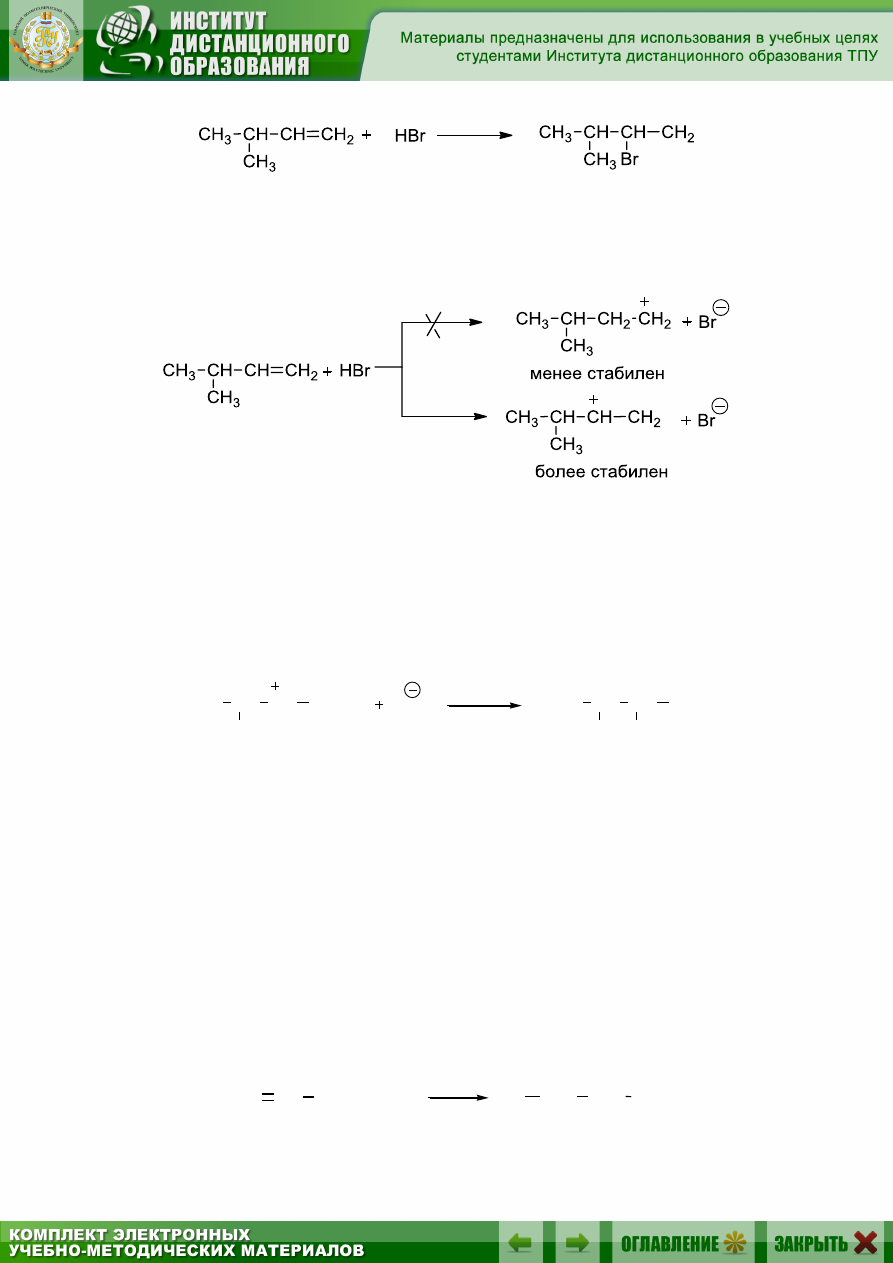
Присоединение галогеноводородов к несимметричным олефинам
происходит в соответствии с правилом В.В. Марковникова (1896): при
ионном присоединении кислоты к двойной углерод-углеродной связи ал-
кена водород присоединяется к атому углерода, который имеет боль-
шее число атомов водорода (который более гидрогенизирован):
97
Такое направление присоединения можно объяснить, исходя из ме-
ханизма электрофильного присоединения галогеноводородов (механизм
A
E
, или Ad
E
). При взаимодействии пропилена с хлороводородом воз-
можно образование двух карбокатионов:
Изопропил-катион более стабилен, чем пропил-катион, благодаря
положительному индукционному эффекту двух метильных групп
и большему эффекту сверхсопряжения (гл. 2). Более устойчивому ка-
тиону соответствует более устойчивое переходное состояние с меньшей
энергией активации. Таким образом, вторичный катион образуется бы-
стрее, чем первичный. Далее более устойчивый катион присоединяет
анион галогена:
CH
2
CH
3
CH CH
CH
3
Br
CH
2
CH
3
CH CH
CH
3
Br
Более точно правило Марковникова можно сформулировать так:
присоединение протона к алкену происходит с образованием наибо-
лее стабильного карбокатиона.
Легкость, с которой различные галогеноводороды присоединяются
к алкенам, зависит от их кислотности и падает в ряду
HI > HBr > HCl > HF.
Это еще раз подтверждает, что лимитирующей стадией в данной
реакции является атака протоном двойной связи.
В редких случаях галогеноводороды присоединятся к алкенам про-
тив правила Марковникова. Подобное присоединение наблюдается, ес-
ли при двойной связи алкена находятся сильные электроноакцепторные
группы, например:
CH
2
CH CF
3
+ HCl
CH
2
CH
2
CF
3
Cl
98
В данном случае, электроноакцепторный заместитель CF
3
, благодаря
сильному –I-эффекту в большей мере дестабилизирует вторичный карбо-
катион CH
3
CH
+
CF
3
, чем первичный
+
CH
2
CH
2
CF
3
, т.к. в последнем группа
CF
3
более удалена от положительно заряженного атома углерода.
6.6.5. Гипогалогенирование. Образование галогенгидринов
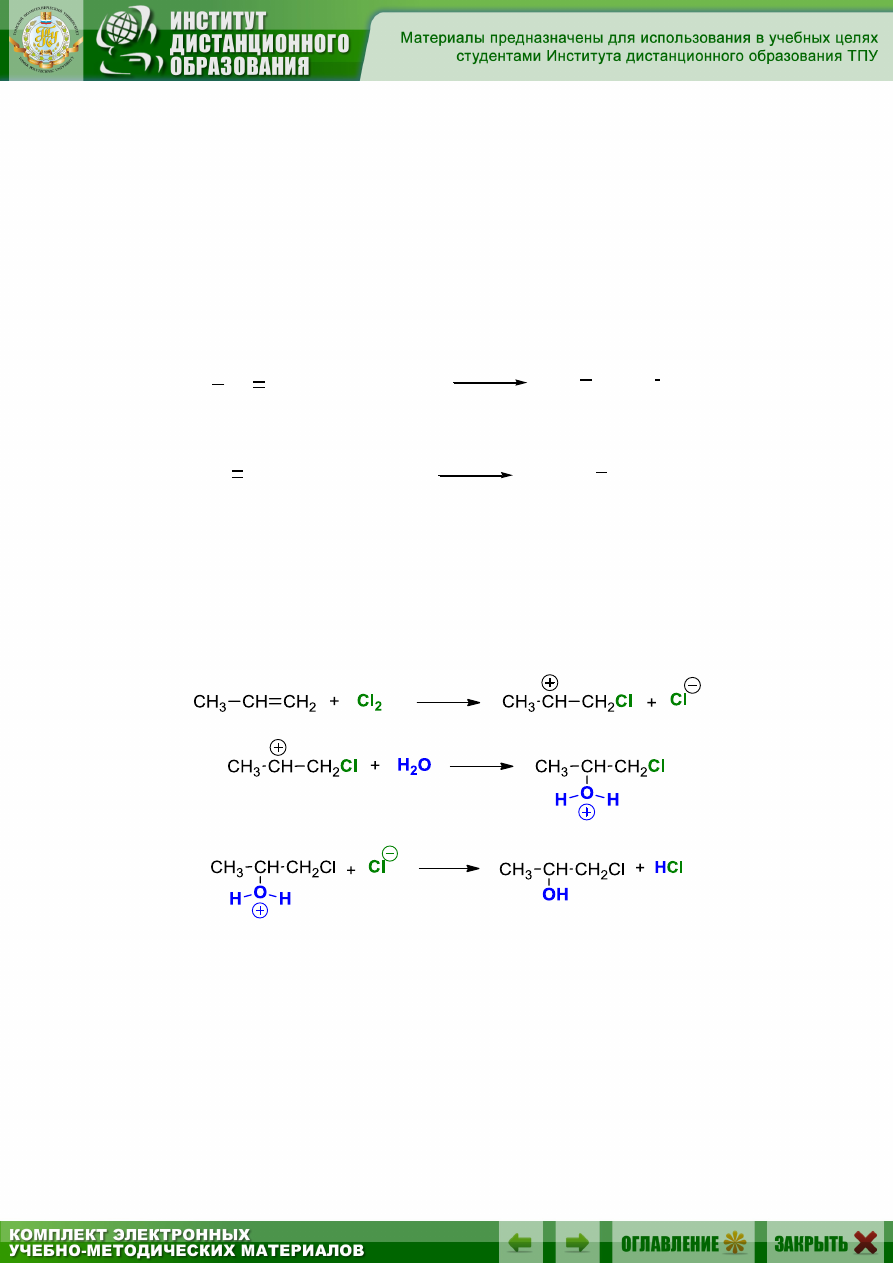
Присоединение хлора или брома в присутствии воды может дать
соединения, содержащие галоген и гидроксильную группу у соседних
атомов углерода. Эти соединения называют галогенгидринами:
Cl
2
+ H
2
O
+
CH CH
2
пропилен
CH
2
OH CH
2
Cl
пропиленхлоргидрин
(1-хлор-2-пропанол)
CH
3
CH
3
Br
2
+ H
2
O
+
CH
2
CH
2
этилен
CH
2
Br CH
2
OH
этиленбромгидрин
(2-бромэтанол)
Реакции протекают, как показано выше, с первоначальной элек-
трофильной атакой галогена на двойную связь и последующим взаимо-
действием образующегося карбокатиона или галогенониевого иона
с нуклеофилом – водой:
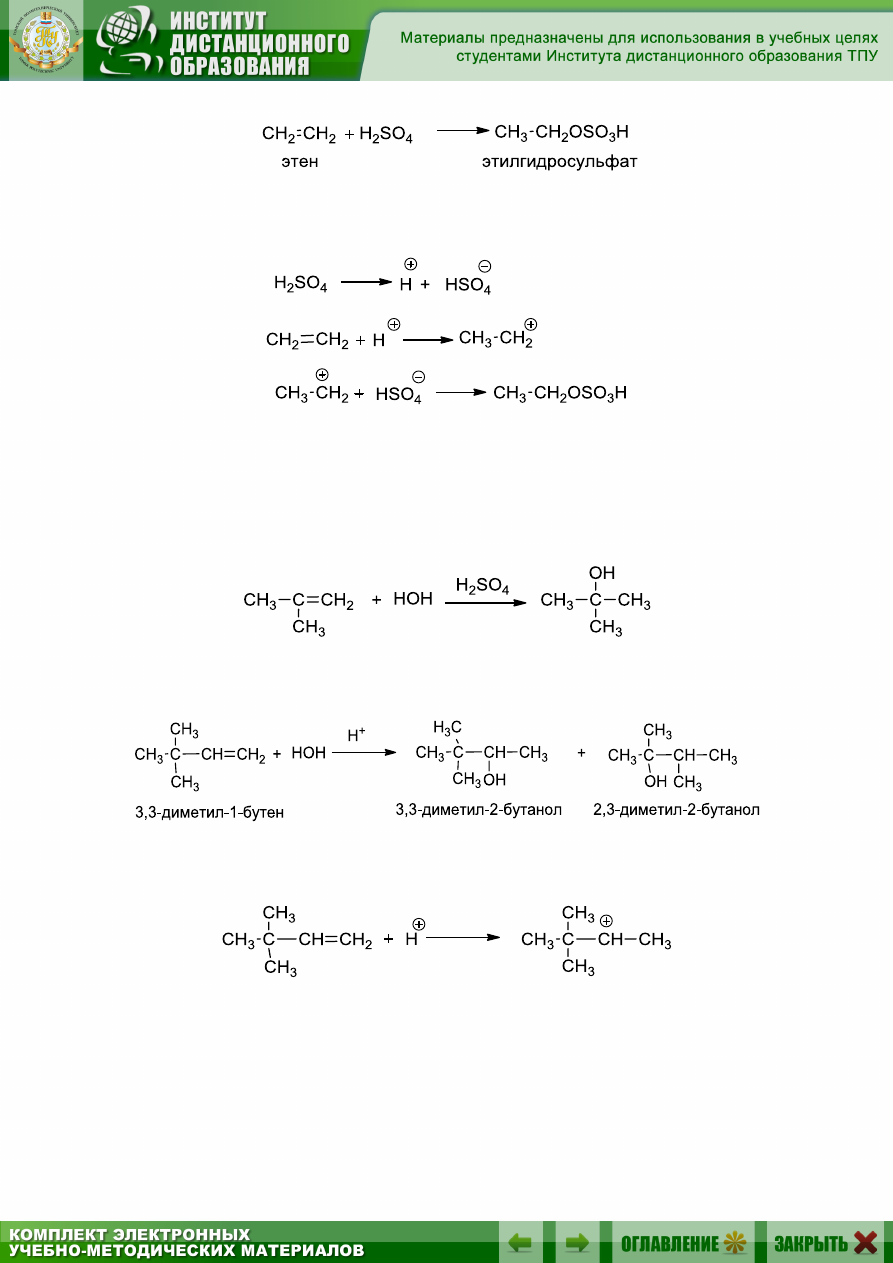
6.6.6. Присоединение серной кислоты
Алкены реагируют на холоду с концентрированной серной кисло-
той с образованием кислых алкилсульфатов общей формулы ROSO
3
H.
Эти вещества образуются в результате присоединения иона водорода
к одному из атомов углерода, связанных двойной связью, а бисульфат-
иона – к другому:
99
Реакция протекает по обычному механизму электрофильного при-
соединения в соответствии с правилом Марковникова:
6.6.7. Гидратация алкенов
При взаимодействии алкена с разбавленным водным раствором ки-
слоты основным продуктом реакции является спирт. Присоединение
протекает по правилу Марковникова:
В некоторых случаях при гидратации алкенов образуется смесь
спиртов:
Для объяснения этого явления рассмотрим механизм гидратации:
1. Реакция начинается с протонирования алкена:
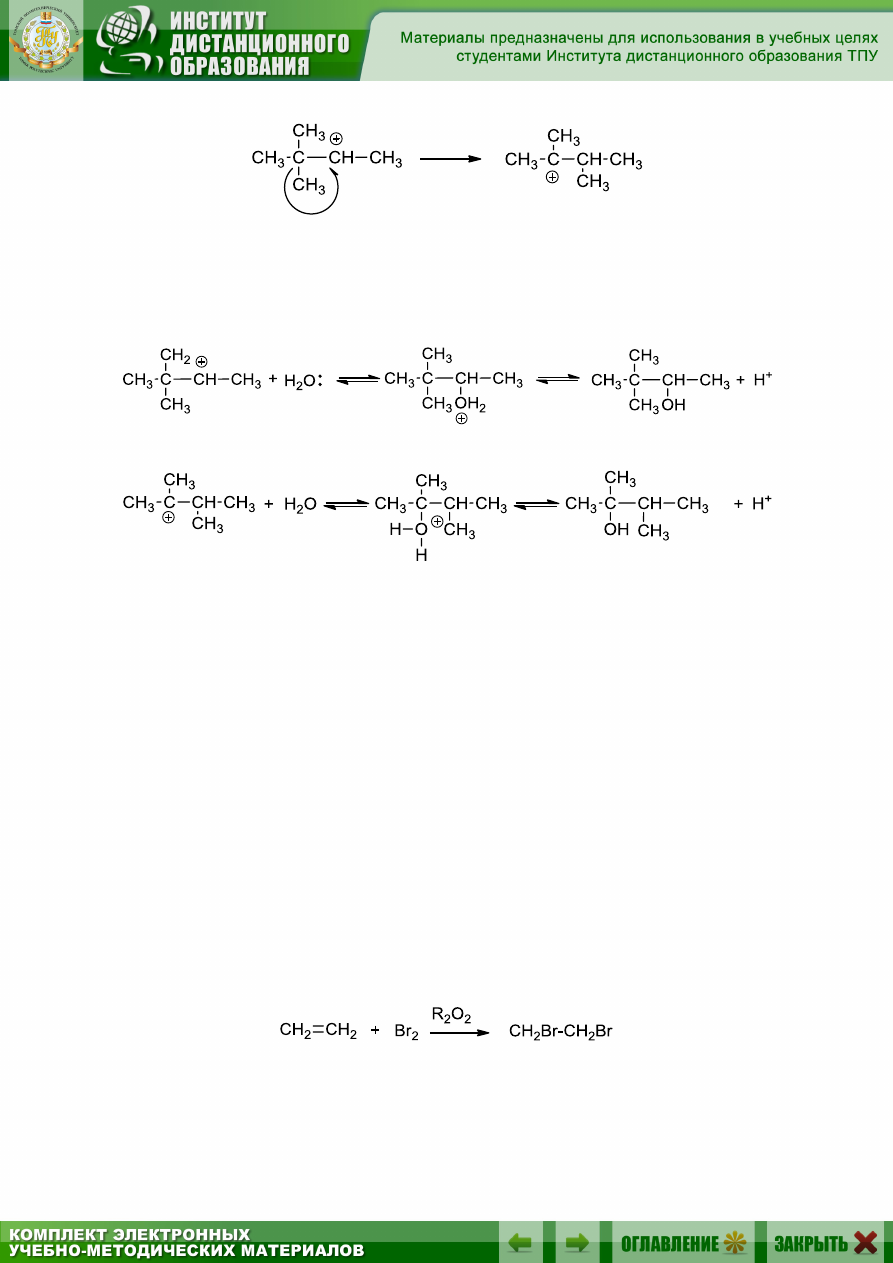
2. Образовавшийся вторичный карбокатион в результате алкильно-
го сдвига частично перегруппировывается в более стабильный третич-
ный карбокатион:
100
Оба карбокатиона реагируют с водой, образуя ионы алкилоксония,
которые, отщепляя протон, превращаются в смесь спиртов с преоблада-
нием третичного спирта:
В целом реакция носит равновесный характер и сдвигается вправо с по-
вышением избытка воды. Гидратация алкенов широко используется
в промышленности для синтеза низших спиртов.
6.6.8. Реакции свободно-радикального присоединения
Свободные радикалы, как и катионы, являются электронодефицит-
ными частицами. Поскольку алкен может предоставить свои
-электроны
для завершения внешней электронной оболочки радикала, закономерна
атака радикалами
-системы двойной связи.
6.6.8.1. Присоединение галогенов
Хлор и бром могут присоединяться к
-связи по свободноради-
кальному механизму, но только в присутствии инициаторов, вызываю-
щих появление свободных радикалов, например при УФ-облучении или
в присутствии пероксидов: