ВУЗ: Московский государственный университет технологий и управления им. К.Г. Разумовского
Категория: Учебное пособие
Дисциплина: Химия
Добавлен: 09.02.2019
Просмотров: 14963
Скачиваний: 28
Монозы существуют в двух формах – линейной (или оксоформе) и
циклической, для описания их строения используют проекции Фишера (для
линейной формы) и проекции Хеуорса (для циклической формы).
Линейные формы моноз
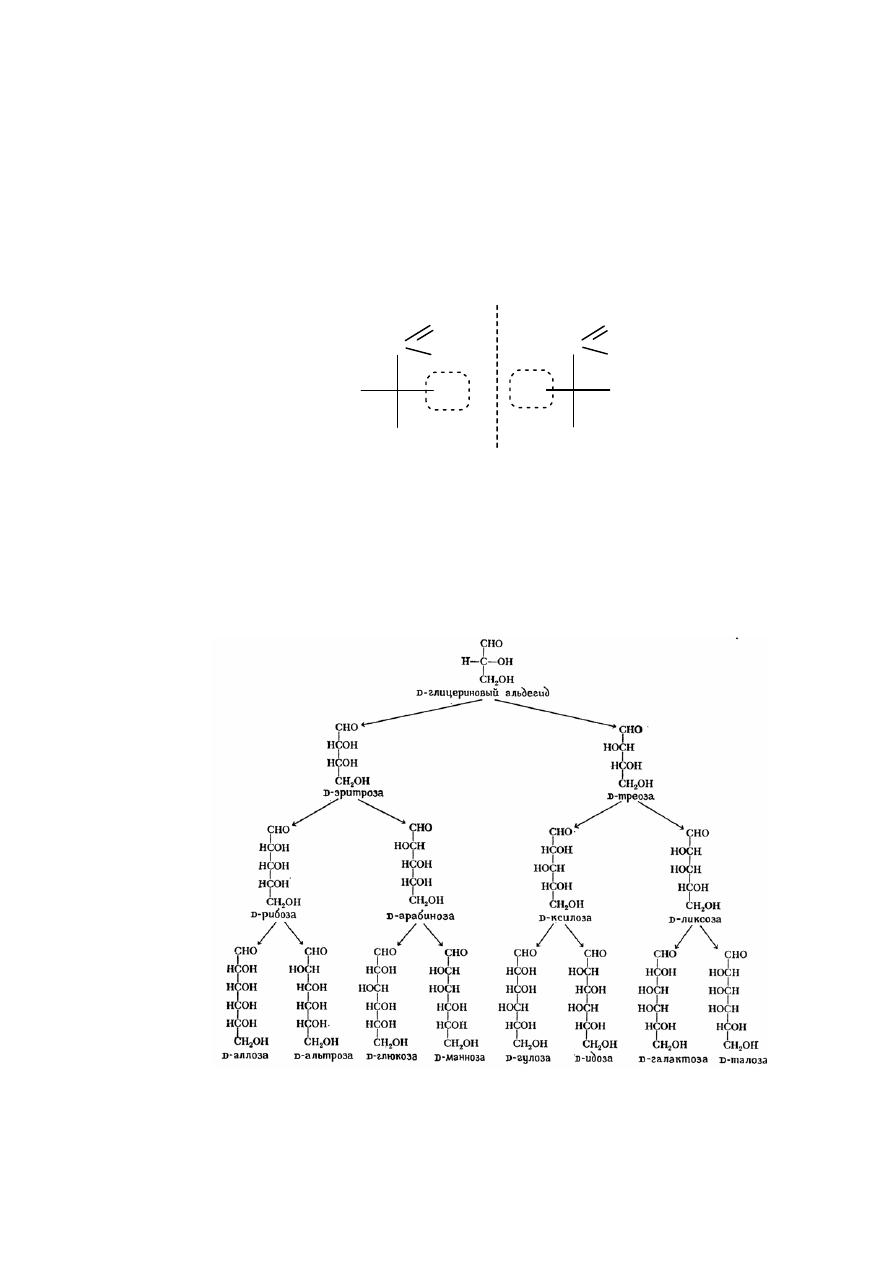
Описывают D и L – ряды моноз. Принадлежность к ряду определяют,
сравнивая конфигурации последнего хирального центра в нижней части монозы
с конфигурацией D- и L – глицериновых альдегидов.
CH
2
OH
OH
H
C
O
H
CH
2
OH
HO
C
O
H
H
D-глицериновый
альдегид
L-глицериновый
альдегид
Линейные формы альдо- и кетотетроз, альдо- и кетопентоз, альдо- и
кетогексоз D-ряда приведены ниже.
Таблица. Ряд D-альдоз
206
Таблица. Ряд D-кетоз
Строение альдогексоз
Линейные формы альдогексоз
Линейные
формы
альдогексоз
являются
стетеоизомерами
пентаоксигексаналя, имеющего четыре асимметрических атомов углерода.
Общая формула:
CH
2
-CH-CH-CH-CH-C
OH OH OH OH OH
O
H
6 5 4 3 2 1
∗
∗
∗
∗
В ряду альдогексоз всего имеется 2
4
=16 стереоизомеров, 8 D,L
(энантиомерных) пар, или 8 диастереомеров (см. таблицу альдогексоз).
Наиболее распространенной в природе альдогексозой является D-глюкоза.
207
OH
H
C
O
H
H
HO
OH
H
OH
H
CH
2
OH
1
2
3
4
5
6
C
CH
2
OH
1
2
3
4
5
6
H
HO
OH
H
H
HO
H
HO
H
O
D-глюкоза
L-глюкоза
∗
∗
По конфигурации пятого асимметрического атома углерода С
5
∗
-
определяют принадлежность альдогексозы к D- или L-рядам, сравнивая с
конфигурацией D- или L- глицеринового альдегида. D- и L-глюкозы являются
энантиомерами.
Кроме D-глюкозы, в природе наиболее часто встречаются D-манноза и D-
галактоза, которые являются диастереомерами.
H
HO
C
O
H
H
HO
OH
H
OH
H
CH
2
OH
1
2
3
4
5
6
C
CH
2
OH
1
2
3
4
5
6
OH
H
H
HO
H
HO
OH
H
H
O
D-манноза D-галактоза
Диастереомеры, способные к взаимному превращению, называются
эпимерами. Эпимеры отличаются по конфигурации у второго асимметричного
атома углерода, следовательно D-глюкоза и D-манноза – эпимеры.
Циклические формы альдогексоз
Полиоксиальдегиды (полиоксикетоны), содержащие пять, шесть и семь
атомов углерода способны к внутримолекулярной циклизации. Циклизация
происходит за счет взаимодействия карбонильной и одной из доступных для
циклизации гидроксильных групп, при этом получаются пяти-, шести- и
семичленные циклические полуацетали (см. тему “Альдегиды, кетоны”).
208
R-C
O
H
+ H
OR
1
+
δ -δ
-
δ
+
δ
H
+
R-CH-OR
1
OH
полуацеталь
R,R
1
- алкилы
Сначала рассмотрим, как происходит циклизация исходя из проекций
Фишера. Напоминаем, что карбонильная группа плоская, следовательно
возможны два варианта атаки гидроксильной группы и образование двух
соединений (см. также циангидридный синтез в теме “Оксикислоты”).
C
O
H
OH
H
H
HO
OH
H
O
H
CH
2
OH
H
-
δ
+
δ
+
δ
-
δ
1
2
3
4
5
6
C
H
OH
OH
H
H
HO
OH
H
H
CH
2
OH
O
1 *
2
3
4
5
6
α-аномер
C
H
HO
OH
H
H
HO
OH
H
H
CH
2
OH
O
1 *
2
3
4
5
6
β-аномер
D-глюкоза
полуацетальный
гидроксил
полуацетальный
гидроксил
В образовавшихся циклических формах (α- и β-) атом углерода С-1
становится асимметрическим атомом углерода, следовательно при наличии
пяти С* существует 2
5
=32 циклические формы альдогексоз D- и L – рядов. α и
β- Формы одной монозы являются диастереомерами и имеет собственное
название - аномеры. У
α-аномера полуацетальный гидроксил и связь С
5
-О
располагаются в цис-конфигурации , а у
β-аномера – в транс-конфигурации.
Для того чтобы перейти от изображения циклической формы в виде
проекции Фишера к более современному изображению в виде проекций
Хеуорса, необходимо выполнить следующее преобразование: произвести две
209
перестановки у пятого С
∗
так, чтобы гидроксильная группа оказалась в нижней
части проекции Фишера (конфигурация этого асимметрического атома
углерода при этом сохраняется). Далее образовать α- и β-циклы.
Проекции Хеуорса изображают в виде шестичленного кольца, нумеруя
асимметрические атомы углерода так, как показано на схеме. Заместители
располагаются на вертикалях. Те заместители, которые находятся слева от
вертикали в проекции Фишера, будут располагаться наверху в проекции
Хеуорса.
C
O
H
OH
H
H
HO
OH
H
H
CH
2
OH
1
2
3
4
5
6
C
O
H
OH
H
H
HO
OH
H
OH
H
CH
2
OH
1
2
3
4
5
6
C
OH
H
H
HO
OH
H
H
CH
2
2
3
4
5
6
O
H
OH
α,β-циклы
- два варианта расположения Н и ОН
OH
OH
две перестановки
у С
5
∗
C
OH
H
H
HO
OH
H
H
CH
2
2
3
4
5
6
OH
O
H
OH
полуацетальный -ОН
переход к
проекции
Хеуорса
наверху в проекции
Хеуорса
O
H
OH
H
OH
OH
H
H
OH
CH
2
OH
6
5
4
3
2
1
α
α-D-глюкопираноза
O
H
H
4H-пиран
полуацетальный ОН
В α-аномере полуацетальный гидроксил расположен под циклом, в β-
аномере – над циклом. Шестичленный кислородсодержащий цикл называется
пираном, отсюда название
α- и β-форм – пиранозы (похожи на пиран).
Название
α- и β-аномеров для D-глюкозы - α-D-глюкопираноза и β-D-
210