Файл: Академика Д. Н. Прянишникова Агрохимический факультет Кафедра агрохимии Ответы на.doc
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 06.11.2023
Просмотров: 497
Скачиваний: 2
СОДЕРЖАНИЕ
1. Предмет агрономической химии. Связь агрохимии с другими науками.
2. Методы агрономической химии.
4. Современное состояние пахотных почв России. Пути выхода из сложившейся ситуации.
6. Питание растений. Типы и виды питания растений.
9. Вынос элементов питания с урожаем (биологический, хозяйственный, остаточный).
14. Избирательная способность растений. Физиологическая реакция удобрений.
15. Периодичность питания растений. Сроки и способы внесения удобрений.
16. Визуальный метод растительной диагностики минерального питания растений.
17. Химический метод растительной диагностики минерального питания растений.
18. Почва как объект изучения агрохимии. Фазовый состав почвы.
19. Минеральная часть твёрдой фазы почвы.
20. Органическая часть твёрдой фазы почвы.
22. Химическая поглотительная способность почвы.
23. Физико-химическая поглотительная способность почвы. Необменное поглощение катионов.
24. Ёмкость катионного обмена почв и состав поглощённых катионов.
28. Агрохимическая характеристика дерново-подзолистых и серых лесных почв.
29. Агрохимическая характеристика чернозёмов и каштановых почв.
32. Значение кальция и магния для растений.
33. Взаимодействие извести с почвой. Влияние извести на свойства почвы.
36. Известковые удобрения. Классификация. Промышленные удобрения (твёрдые известковые породы).
38. Место внесения извести в севообороте. Сроки и способы внесения известковых удобрений.
41. Определение доз гипса. Мелиоративные материалы, используемые для гипсования.
43. Значение серы для растений. Удобрение гипсом бобовых трав.
44. Классификация минеральных удобрений. Физико-механические свойства минеральных удобрений.
Признаки недостатка и избытка азота для растений.
47. Содержание и формы азота в почвах.
51. Источники получения, классификация и ассортимент азотных удобрений.
52. Нитратные удобрения. Состав. Получение. Свойства. Взаимодействие с почвой. Применение.
53. Аммонийные удобрения. Состав. Получение. Свойства. Взаимодействие с почвой. Применение.
54. Аммонийно-нитратные удобрения. Состав. Получение. Свойства. Взаимодействие с почвой. Применение.
55. Аммиачные удобрения. Состав. Получение. Свойства. Взаимодействие с почвой. Применение.
56. Амидные удобрения. Состав. Получение. Свойства. Взаимодействие с почвой. Применение.
58. Ингибиторы нитрификации. Коэффициенты использования азота из минеральных удобрений.
59. Дозы, сроки и способы внесения азотных удобрений.
60. Эффективность азотных удобрений. Экологические аспекты применения азотных удобрений.
25. Реакция почвы (кислотность, щёлочность). Принципы методов определения обменной (рНKCl) и гидролитической кислотности почв.
Реакция почвы – это обусловленная состоянием поглощенных катионов способность почвы подкислять или подщелачивать взаимодействующие с ней растворы солей или воду. Кислотность почв подразделяется на актуальную и потенциальную. Актуальная (активная) кислотность обуславливает повышение концентрации катионов Н в почвенном растворе и определяется водной вытяжкой из почвы (рНн2о). Потенциальная (пассивная) кислотность обусловлена наличием катионов H, Al, Fe в ППК, т.е. в твердой фазе почвы.
Обменная кислотность почв. Принцип потенциометрического метода определения обменной кислотности (рНКСL) почв.
В зависимости от способа определения потенциальной кислотности различают обменную и гидролитическую формы потенциальной кислотности. Обменная кислотность создается Н, Al, Fe (более подвижными) способными вытесняться в раствор при действии на почву гидролитически нейтральных солей (в т.ч. удобрений NaNO3, K2SO4 и др.)
Общепринятый метод – обработка почвы 1н. раствором, KCl (рН=5,5-5,8).
Реакции:
Al 3К
ППК)Н + nKCl = ППК)К + (n – 7)KCl + HCl + AlCl3 + FeCl3
Fe 3К
AlCl3 + 3Н2О = Al(OH)3 + 3HCl
FeCl3 + 3Н2О = Fe(OH)3 + 3HCl
Чаще всего обменная кислотность выражается как рНkcl, или м-экв/100 г почвы. При определении обменной кислотности учитываются катионы Н находящиеся в почвенном растворе, т.е. в величину обменной кислотности входит и актуальная кислотность. Между ППК и почвенным раствором существует динамическое равновесие, поэтому при внесении в почву удобрений. Обменная кислотность может переходить в актуальную, ухудшая условия развития растений. Обменная кислотность характерна для подзолистых, дерново-подзолистых, красноземов, а также почв северной части черноземной зоны (серые лесные, выщелоченные черноземы). По величине рНkcl определяется степень кислотности почв и нуждаемость их в известковании, очередность известкования и дозы извести.
Группировка почв по степени кислотности солевой вытяжки
| № группы | Рекомендуемый цвет окраски | Почвы по степени кислотности | рНKCl |
| 1 | Красный | Очень сильнокислые | < 4,0 |
| 2 | Розовый | Сильнокислые | 4,1-4,5 |
| 3 | Оранжевый | Среднекислые | 4,6-5,0 |
| 4 | Желтый | Слабокислые | 5,1-5,5 |
| 5 | Светло-зеленый | Близкие к нейтральным | 5,6-6,0 |
| 6 | Зеленый | Нейтральные | > 6,0 |
Гидролитическая кислотность почв.
Гидролитическая кислотность обусловлена Н, Al, Fe (более прочно связанными с ППК) не вытесняющимися раствором нейтральной соли. Определяется обработкой почвы раствором гидролитически щелочной соли: 1н. CH3COONa.
Реакции:
Al 3Na
ППК)Н + nCH3COONa = ППК)Na + (n – 7)CH3COONa + 7CH3COOH + Al(ОН)3 + Fe(ОН)3
Fe 3Na
Гидролитическая кислотность выражается в м-экв/100 г почвы. Включает в себя: актуальную, обменную, и собственно гидролитическую. Собственно гидролитическая характеризуется слабой подвижностью и в отсутствии актуальной и обменной форм (например в черноземах) не оказывает вредного влияния на растения.
Щёлочность почв.
В щелочных почвах (ю. черноземах, каштановых, солонцах)
Выделяют:
1) Актуальная
2) Потенциальная
Актуальная обусловлена наличием в растворе гидролитически щелочных солей. Определяется при обработке почвы водой и выражается в рНн2о или м-экв/100 г почвы. Потенциальная связана с нахождением ионов Na в ППК. По величине щелочности определяют нуждаемость почв в гипсовании, а по доле Na в ППК рассчитывают дозы гипса. Реакция почвы оказывает большое влияние на агрохимические, агрофизические свойства почв, превращение питательных веществ, жизнь м.о. Приемы химической мелиорации направлены на создание слабокислой или нейтральной реакции среды, благоприятной для большинства растений.
1. Определение обменной кислотности (рНkcl) потенциометрически
Значение анализа: обменная кислотность - наиболее вредная для растений форма почвенной кислотности, обусловленная более подвижными ионами, водорода и алюминия почвенного поглощающего комплекса (ППК), способными вытесняться в раствор при действии на почву гидролитически нейтральной соли. По величине обменной кислотности, используя группировку, представленную ниже, можно определить степень кислотности почвы и нуждаемость её в известковании. Показатель pHkcl используется при определении доз извести.
Принцип метода: катионы водорода и алюминия вытесняются из почвенного поглощающего комплекса с помощью гидролитически нейтральной соли 1 н. раствора хлорида калия (КCl), рН которого составляет 5,5-5,8 при соотношении почвы к раствору 1: 2,5. При этом происходят следующие реакции:
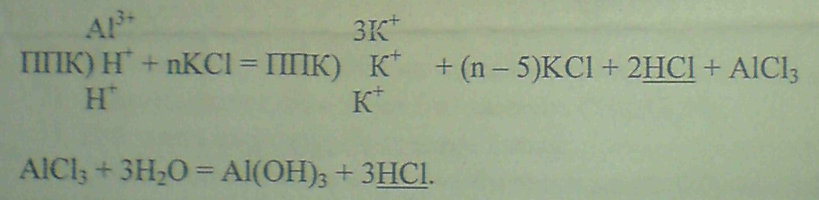
Значение рН полученной вытяжки определяется потенциометрически с помощью селективного по отношению к катионам водорода стеклянного электрода.
2. Определение гидролитической кислотности (Нг) по Каппену
Значение анализа: гидролитическая кислотность - максимальная форма почвенной кислотности, характеризующая весь поглощённый водород. Гидролитическая кислотность обусловлена ионами водорода, более прочно связанными с коллоидами почвы и не вытесняющимися из почвенного поглощающего комплекса (ППК) раствором нейтральной соли. Она определяется при обработке почвы раствором гидролитически щелочной соли. При сопоставлении значений гидролитической кислотности и суммы поглощённых оснований можно сделать предположение о степени кислотности почв. Гидролитическая кислотность используется при расчёте ёмкости катионного обмена, степени насыщенности почв основаниями, определении доз извести и возможности применения фосфоритной муки в чистом виде.
Принцип метода: катионы водорода вытесняются из почвенного поглощающего комплекса с помощью гидролитически щелочной соли - 1 н. раствора ацетата натрия (СН3СООН), рН которого составляет 8,0-8,2 - при соотношении почвы к раствору 1: 2,5. При этом происходит следующая реакция:
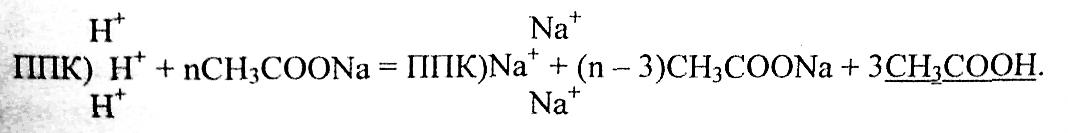
По количеству 0,1 н. раствора гидроксида натрия (NaOH), пошедшего на титрование образовавшейся уксусной кислоты (СНзСООН), рассчитывается гидролитическая кислотность.
26. Сумма поглощённых оснований и степень насыщенности ими почв. Принцип метода определения суммы поглощённых оснований в почвах.
Общее содержание в ППК катионов кроме H,Al,Fe выражается м-экв/100 г почвы, обозначается S.
Формула для расчета суммы поглощенных оснований:
а – объем фильтрата взятого для титрования
к1 – поправка к титру HCl
b – количество NaOH пошедшее на титрование
к2 – поправка к титру NaOH
0,1 – нормальность растворов
100 – пересчет на 100 г почвы
Н – навеска почвы соответствующая взятому объему фильтрата
Степень насыщенности почв основаниями показывает сколько % общей емкости поглощения занимают основания. V является важным агрохимическим показателем позволяющим определить степень нуждаемости почв в известковании. Чем выше V тем ниже кислотность и нуждаемость в известковании.
Формула для расчета степени насыщенности почв основаниями:
Определение суммы поглощённых оснований (S) по Каппену-Гильковицу
Значение анализа: сумма поглощённых оснований показывает общее содержание катионов оснований (Са +, Mg2+, К+, Na+, NH4 и т.д.) в почвенном поглощающем комплексе (ППК). При сопоставлении значений суммы поглощённых оснований и гидролитической кислотности можно сделать предположение о степени кислотности почв. Этот показатель необходим для расчёта ёмкости катионного обмена и степени насыщенности почв основаниями.
Принцип метода: катионы оснований вытесняются из почвенного поглощающего комплекса с помощью 0,1 н. раствора соляной кислоты (HCI) при соотношении почвы к раствору 1: 5. При этом происходит следующая реакция:
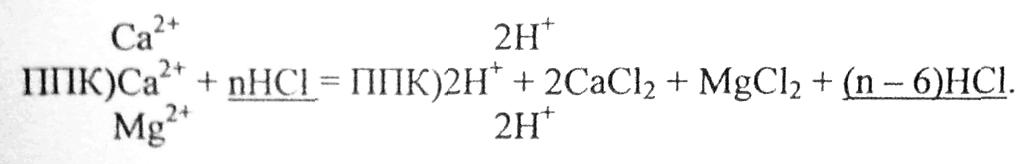
В результате обменной реакции нейтрализуется количество кислоты, эквивалентное количеству поглощённых оснований. Остаток кислоты учитывается титрованием 0,1 н. раствором гидроксида натрия (NaOH). Сумма поглощённых оснований рассчитывается по разности между исходным и оставшимся количеством кислоты.