Файл: Упр 1 Приведите примеры технических устройств, действие которых основано на открытии радиоактивности, электромагнитных волн, ультразвука, реактивного движения.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 10.11.2023
Просмотров: 144
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
p*V1*Δt*S1=p*V2*Δt*S2
S2=S1*V1/V2=S1*√2*g*h1/√2*g*(h1+h2)=S1*√(h1/(h1+h2)=1*√20/70=0,53 см2
2. На какой высоте площадь поперечного сечения вертикальной струи
фонтана в 3 раза больше выходного отверстия трубки? Скорость воды
в выходном отверстии 9 км/ч. Сопротивление воздуха не учитывать
сечения струи фонтана будет в 5 раз больше площади выходного отверстия трубки? Скорость воды в выходном отверстии 10м/с
дано V1=10 м/с S2/S1=5 h- ?
так как объемы одинаковые
V1*S1*t=V2*S2*t
V1/V2=S2/S1=5
V2=2 м/с
h=V2^2-V1^2)/-2*g=(4-100)/19,6=4,9 м
3. В водопроводной трубе образовалось отверстие сечением 4 мм 2 , из кото-
рого вертикально вверх бьет струя воды, поднимаясь на высоту 80 см.
Какова утечка воды за сутки
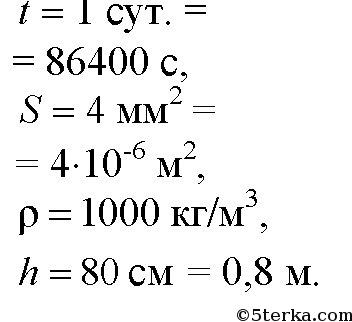
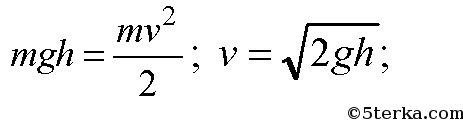
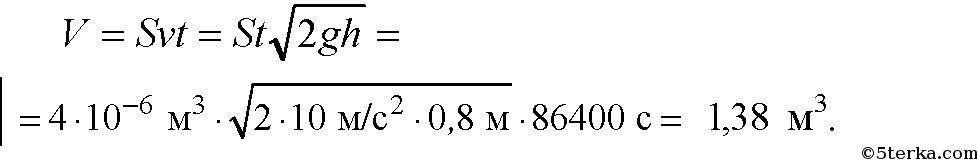
4. Шарик всплывает в жидкости, плотность которой в 4 раза больше плот-
ности материала шарика с постоянной скоростью. Во сколько раз сила
трения, действующая на шарик, больше веса этого шарика?
Дано:
| ρ1 = 4 ρ2 v = const |
| Fтp/ mg - ? |

5. Какой наибольшей скорости может достичь дождевая капля диаметром
d = 0,3 мм, если динамическая вязкость воздуха равна 1,2 · 10 –5 Па · с

6. Стальной шарик диаметром 1 мм падает с постоянной скоростью
0,185 см/с в большом сосуде, наполненном касторовым маслом. Опреде-
лите динамическую вязкость касторового масла. Плотность касторового
масла 900 кг/ м 3
ешение:
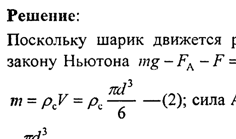 |  |
 | 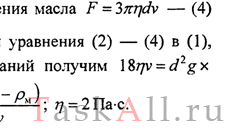 |
упр 17
-
Масса 14,92·10 25 молекул инертного газа составляет 5 кг. Какой это газ?
N/Na=m/M
Na-Число Авогадро
M-Молярная масса молекулы
M=Na*m/N
M=6.02*10^23*5/14.92*10^25= 20 г/моль (Неон)
2,,В устье Амазонки найден один из крупных самородков золота массой
62,3 кг. Какие количества вещества в нем содержится
V=m/M V-кол-во вещества M=197/1000=0.197кг/моль V=62.3/0.197=316.2моль
3. Капля минерального масла плотностью ρ = 920и массой 0,023 мг,
вылитая на поверхность воды, образовала пленку площадью 60 см 2 . Пред-
полагая, что молекулы в пленке расположились в один ряд, определите
диаметры молекул
V=m/p V=S*d d- поперечник молекулы. mp=S*d d=m/S*p=0,023*10^-6/60*10^-4*920=4,16*10^-9 м
4. Плотность алюминия 2 7 10 3 Какое количество вещества содержится
в 1 м 3 алюминия?
Количество вещества v=m/M M=27*10^-3 кг/моль
масса вещества m=p*V
v=p*V/M=2,7*10^3*1/27*10^-3=10^5 моль
5. Какой скоростью обладали молекулы паров серебра, если их угловое смещение в опыте Штерна составило 5,4° при частоте вращения прибора
150 с –1 ? Расстояние между внешним и внутренним цилиндрами равно 2 см.
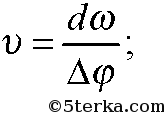
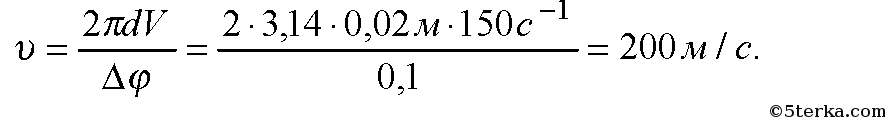
Упр 18
1. Выразите в Кельвинах следующие значения температур: 20 °C, 27 °C,
–73 °C, 100 °C.
Ответ:0с=273К
300 K; 373; 400; 200; 50; 73
Объяснение:
К количеству C прибавляй 273 и все
Например: 27С это 27+273=300
2. Выразите в градусах Цельсия следующие температуры: 4 K, 200 K, 440 K,
300 К.
3. Определите температуру по шкале Цельсия, если по шкале Фаренгейта
температура равна: 84,2 °F, 80,6 °F, 71,6 °F.
4-273 = -269 С
180-273=-93 С
310-273=37 С
420-273=147 С
4. Переведите в градусы по шкале Фаренгейта температуры: 30 °C, 25 °C, 20 °C
1) 86
2)77
3)68
Упр 19
1. В сосуде объемом V = 1 л находится водород массой 2 г. Определите дав-
ление водорода, если средняя квадратичная скорость его молекул
u=400м/с
По закону Менделеева-Клапейрона:
p*V=m*R*T/M
Но
Vкв=√(3*R*T/M)
Vкв²=3*R*T/M
R*T/M = Vкв² /3
Тогда:
p*V=m*Vкв²/3
p=m*Vкв²/(3*V)
p=0,002*400²/(3*1*10⁻³) ≈ 110 000 Па = 1,1*10⁵ Па
2. Плотность водорода при некоторых условиях равна 0,09кг/м3 Опреде-
лите молярную массу метана, если его плотность при тех же условиях 0,72кг/м3
Дано:
р1(ро)= 0.09кг/м3
р2=0.72кг/м3
М(СН4)-?
Анализ:
М=Мr*10(-3) степени кг/м
Решение:
Mr(CH4=12+4*1=16
М=16*10(-3)степени кг/м
3. Газ плотностью r=3,3кг/м3 находится при температуре t C = ° 17 . Опреде-
лите давление газа, если масса молекулы m 0 = 6,6·10 – 27 кг. Какой это газ?
Уравнение М-К: PVM=mRT; плотность=m / V. Для нахождения М дана масса молекулы, её нужно * на число Авогадро (6,02*10 в 23 степени) . Не забудьте всё делать в системе СИ, температура, например д. б. 273К; R=8,31
4. Определите температуру N = 2·10 22 молекул идеального газа, находяще-
гося в сосуде емкостью V = 13,8 л при давлении р =100 кПа.
Концентрация молекул n=N/V
P=n*k*T
P=N*k*T/V
T=P*V/N*k=10^5*13,8*10^-3/2*10^22*1,38*10^-23=5*10^3 K
5. Определите концентрацию молекул идеального газа, если при темпера-
туре Т = 300 К плотность газа 1,2кг/м3 а средняя квадратичная скорость 500м/с

упр 20
1. Определите температуру аммиака NH3, находящегося под давлением
2,3 · 10 5 Па, если его объем 0,02 м 3 , а масса 30 г.
РV=mRT/M PVM=mRT T=PVM/mR=210000*0.02*0.017/0.03*8.31=286[K]
2. Какое количество вещества находится в баллоне вместимостью 10 л при
давлении 0,29 МПа и температуре 17 °С?

3. Определите плотность кислорода при температуре 47 °С и атмосферном
давлении 10 5 Па.
P*V*M=m*R*T p=m/V
P*M=p*R*T
p=P*M/R*T=10^5*32*10^-3/8,31*320=1,2 кг/м3
4. Сколько молекул заключено в объеме 0,5 м 3 газа, если при температуре
300 К он находится под давлением 7,48 · 10 5 Па?
Запишем уравнение Менделеева-Клапейрона: pV = vRT
v = N/Na
v = pV / RT = 7,5*10⁵*0,5 / 8,31*300 = 150,4 моль
N = v*Na = 150,4 * 6,02 * 10²³ = 9,05 *10²⁵
5. Давление газа при уменьшении его объема в 2 раза увеличилось на 120 кПа,
а абсолютная температура возросла на 10 %. Каким было первоначальное
давление?
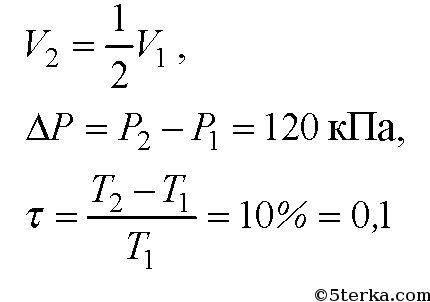
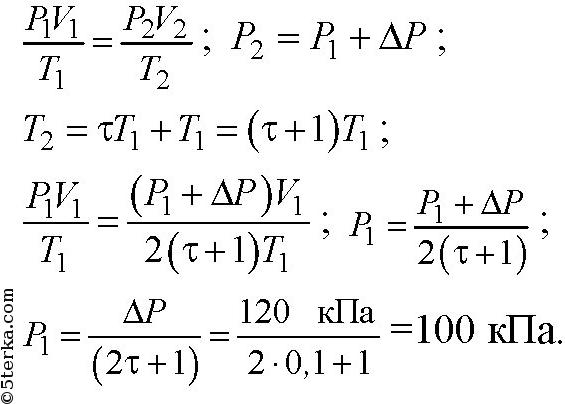
6. В баллоне находится газ с температурой 15 °С. Во сколько раз уменьшится
давление газа, если 40 % выйдет из баллона, а температура при этом пони-
зится на 8 °С?
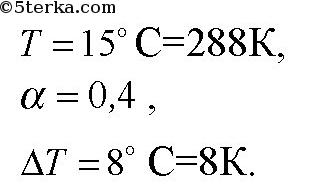
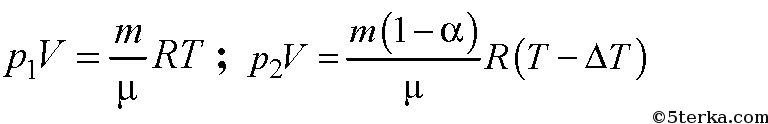
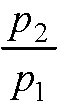
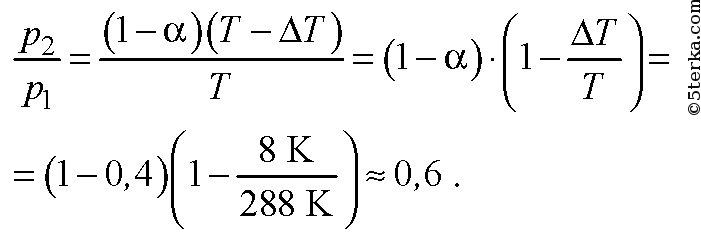
Упр 21
-
Сосуд, содержащий 10 л воздуха при дав- лении 1 МПа, соединяют с пустым сосудом вместимостью 4 л. Определите давление, установившееся в сосудах. Процесс изотер- мический.
P1=p0v0/v0+v=714 кПа
-
При 27 оС газ занимает объем 10 л. До какой температуры его следует изобарно охладить, чтобы объем уменьшился на 0,25 первона- чального объема?
T1 =27 C = (27+273) =300 K
V1 = 10 л
V2 = V1 - 0.25 V1 = 0.75 V1 = 7.5 л
---------------------
T2 - ?
РЕШЕНИЕ
PV = vRTизобарный процесс - определим константу
V/T = vR/P <---константа
тогда V1 / T1 = V2 /T2
T2 = V2 / V1 *T1 = 7.5 /10 *300 =225 К
Упр 22
-
Как изменится внутренняя энергия 240 г кисло- рода при его охлаждении на 100 K?
Решение:
Исходя из этой пропорции, масса равна
M= кг/моль
- 1 2 3 4 5 6 7 8
Определите внутреннюю энергию одноатом- ного идеального газа, взятого в количестве 5 молей, при температуре 27 °С?
U = i/2*v*R*T
i=3 - для одноатомного газа
v = 5 моль
T=273+27=300 К
U = i/2*v*R*T = 3/2 * 5 * 8,31 * 300 Дж = 18 698 Дж
18,7 КДж
-
Зависит ли изменение внутренней энергии газа от способа его перевода из состояния 1 в состо- яние 2 (рис. 119)? Найдите изменение внутренней энергии при переходе из состояния 1 в состояние 2, если газ одноатомный; p0 = 105Па, V0 = 2 л.
p1=3*10^4 Па V1=4 м3 р2=6*10^4 Па V2=12 м3 ΔU=?
ΔU=(i/2)*v*R*ΔT Для 2-х атомных газов i=5
Работа газа A=(p1+p2)*(V2-V1)/2=v*R*ΔT (графически - работа равна площади трапеции).
ΔU=(5/4)*p1+p2)*(V2-V1)=(5/4)*(6+3)*(12-4)*10^4=0,9*10^6 Дж
-
Один моль газа, имевший начальную температуру Т = 300 К, изобарно расширился, совершив работу А = 12,5·103 Дж. Во сколько раз при этом увеличится объем газа?
Определите внутреннюю энергию одноатом- ного идеального газа, взятого в количестве 5 молей, при температуре 27 °С?
U = i/2*v*R*T
i=3 - для одноатомного газа
v = 5 моль
T=273+27=300 К
U = i/2*v*R*T = 3/2 * 5 * 8,31 * 300 Дж = 18 698 Дж
Зависит ли изменение внутренней энергии газа от способа его перевода из состояния 1 в состо- яние 2 (рис. 119)? Найдите изменение внутренней энергии при переходе из состояния 1 в состояние 2, если газ одноатомный; p0 = 105Па, V0 = 2 л.
Один моль газа, имевший начальную температуру Т = 300 К, изобарно расширился, совершив работу А = 12,5·103 Дж. Во сколько раз при этом увеличится объем газа?
| Дано:
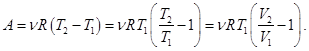 | Решение: : |
Упр 23
-
Для изобарного нагревания 800 молей газа на 500 К сообщили 9,4 МДж теплоты. Определите работу газа и изменение внутренней энергии.