Файл: Правила проведения суммативного оценивания 5 Модерация и выставление баллов 5.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 06.12.2023
Просмотров: 319
Скачиваний: 7
СОДЕРЖАНИЕ
Правила проведения суммативного оценивания
СПЕЦИФИКАЦИЯ СУММАТИВНОГО ОЦЕНИВАНИЯ ЗА 1 ЧЕТВЕРТЬ
Структура суммативного оценивания
Характеристика заданий суммативного оценивания за 1 четверть
CПЕЦИФИКАЦИЯ СУММАТИВНОГО ОЦЕНИВАНИЯ ЗА 2 ЧЕТВЕРТЬ
Обзор суммативного оценивания за 2 четверть
Количество баллов –30 Типы заданий:
Структура суммативного оценивания
Характеристика заданий суммативного оценивания за 2 четверть
СПЕЦИФИКАЦИЯ СУММАТИВНОГО ОЦЕНИВАНИЯ ЗА 3 ЧЕТВЕРТЬ
Обзор суммативного оценивания за 3 четверть
Структура суммативного оценивания
Характеристика заданий суммативного оценивания за 3 четверть
СПЕЦИФИКАЦИЯ СУММАТИВНОГО ОЦЕНИВАНИЯ ЗА 4 ЧЕТВЕРТЬ
Обзор суммативного оценивания за 4 четверть
Структура суммативного оценивания
Характеристика заданий суммативного оценивания за 4 четверть
-
Карбоновые кислоты – органические вещества, способные проявлять свойства, схожие со свойствами неорганических кислот. К примеру, уксусная кислота нейтрализует гидроксид натрия с образованием средней соли - ацетата натрия CH3COONa. При выпечке кондитерских изделий соду (NaHCO3) «гасят» уксусной кислотой. В этом случае используется другое свойство кислот – способность реагировать с солями более слабых кислот. Запишите уравнения перечисленных реакций.
[2]
| 9. | Специфическим свойством карбоновых кислот является способность образовывать сложные эфиры. При взаимодействии пропилового спирта и уксусной кислоты образуется Н+ эфир с запахом груши СН3СООН + С3Н7ОН → СН3СООС3Н7 + Н2О Запишите механизм данной реакции. [3] |
| 10. |
Заполните схему классификации жиров: ЖИРЫ по происхождению по агрегатному состоянию по составу Глицерин + Глицерин + [3]
[1] В 1912г. Поль Сабатье был удостоен Нобелевской премии за открытие катализатора (мелкоизмельченный металлический никель или платина) для процесса получения искусственного твердого жира – саломаса, идущего на изготовление маргарина и заменителей сливочного масла.
[1] В 1808 году французский химик М. Э. Шеврель установил, что мыло – это натриевая соль высшей жирной кислоты. Он изготовил мыла из различных жиров реакцией щелочного гидролиза или «омыления» жиров.
[1] [Всего 30 баллов] |

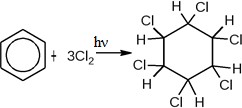 Схема выставления баллов
Схема выставления баллов
| № | Ответ | Балл | Дополнительная информация |
| 1 | В | 1 | |
| 2 | С | 1 | |
| 3 | В | 1 | |
| 4(a) | В молекуле бензола каждый атом углерода находится в состоянии sp2-гибридизации и связан тремя - связями с двумя атомами углерода и одним атомом водорода. Четвертый валентный электрон атома углерода находится на p-орбитали, перпендикулярной плоскости молекулы. В молекуле бензола происходит боковое перекрывание р-орбиталей каждого атома углерода с р-орбиталями обоих соседних атомов углерода. В результате такого сопряжения образуется единое -электронное облако, расположенное над и под плоскостью бензольного кольца – осуществляется круговое сопряжение. Такая циклическая система с общим облаком из шести электронов очень устойчива, энергетически выгодна; поэтому бензол преимущественно вступает в те реакции, в которых ароматическое кольцо сохраняется. | 1 | |
| 4(b) | 1. 2. 3. | 1 1 1 | |
| 5(a) | Для того чтобы избежать разбавления азотной кислоты выделяющейся во время нитрования водой, азотную кислоту применяют в смеси с веществами, связывающими воду. Для этого чаще всего применяют концентрированную серную кислоту, смесь которой с концентрированной азотной кислотой называется «нитрующей смесью». | 1 | |
| 5(b) | Механизм нитрования бензола: HNO3 + 2H2SO4 → Н3О + + NO2 + + 2HSO4 ‾ | 1 | |
| | 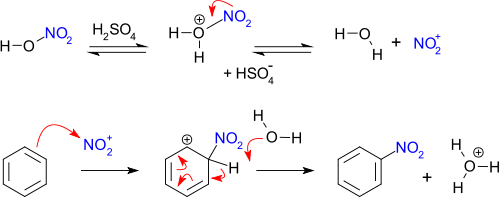 | 1 1 | |
| 6(a) | метильная группа СH3 (за счет +I-эффекта) повышает электронную плотность в бензольном кольце в положениях 2, 4 и 6: 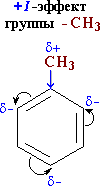 и облегчает замещение именно в этих положениях. Под влиянием бензольного кольца метильная группа СH3 в толуоле становится более активной в реакциях окисления и радикального замещения по сравнению с метаном СH4 | 1 1 | 1 балл – обозначение положений 1 балл – схема распределения |
| 6(b) | Например, при нитровании толуола С6Н5CH3 происходит замещение не одного, а трех атомов водорода с образованием 2,4,6-тринитротолуола: 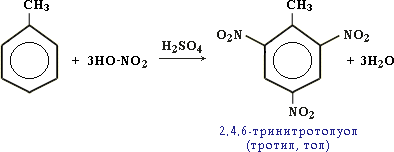 | 1 | |
| 6(c) | Толуол, в отличие от метана, окисляется в мягких условиях (обесцвечивает подкисленный раствор KMnO4 при нагревании): 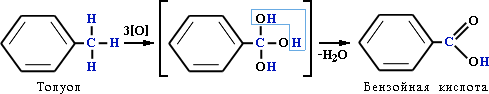 | 1 | |
| 7(a) | | реагент вещество | качественный реагент | наблюдае мый эффект | | 1 1 | 1 балл за каждую правильно заполненную строку/столбец | ||
| пропаналь | С аммиачным раствором оксида серебра (реакциясеребряногозеркала). [Ag(NH3)2]OH | Налет серебра | |||||||
| диметилкет он | Только в присутвтсии сильных окислителей и нагревании | При обычных условиях не окисляют ся | |||||||
| 7(b) | A-3, B-4 | 2 | | ||||||
| 8 | 1)2CН3СOOH+2NaOH=2CH3COONa + H2 2) CН3СOOH+NaHCO3=CH3COONa + H2O+CO2 | 1 1 | | ||||||
| 9 | 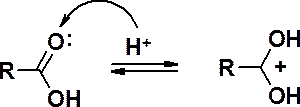 R-CH3 ; R' –C3H7 | 1 | | ||||||
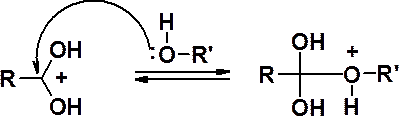 | 1 | ||||||||
| | 1 | ||||||||
| 10(a) | Животные Растительные Твердые Жидкий (искл.рыбный) (искл.кокосовое) Глицерин + Глицерин + высш.насыщ к/к высш.НЕнасыщ к/к | 3 | 1 балл за каждые 2 правильных ответа | ||||||
| 10(b) | 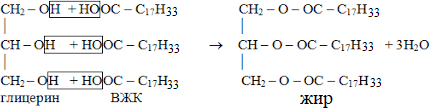 | 1 | | ||||||
| 10(c) | 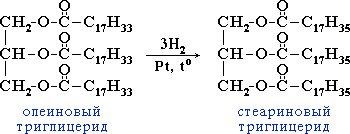 | 1 | |
| 10(d) | 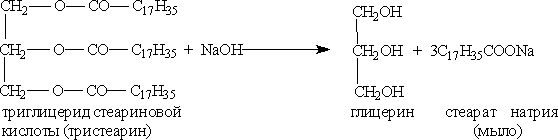 | 1 | |
| | | 30 | |