Файл: Конспект лекций для студентов специальности 1 48 01 02 Химическая технология органических веществ, материалов и изделий.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.01.2024
Просмотров: 1255
Скачиваний: 1
СОДЕРЖАНИЕ
Основные понятия и определения
Направленность ковалентной связи. Гибридизация орбиталей
Насыщаемость ковалентной связи
5 Общие свойства растворов. Идеальные растворы. Законы Рауля
Если в раствор добавить, например гидроксид натрия
Влияние pH на растворимость электролитов
Преимущественное направление ионно-молекулярных реакций
Получение заданного вещества реакцией обмена
Восстановители-металлы (простые вещества)
Составление материального баланса в полуреакциях
Комплексные соединения в окислительно-восстановительных реакциях
Электронный баланс в полуреакциях
Уравнение Нернста для металлического электрода
Электрохимический ряд металлов
Материальный баланс электрохимических реакций. Законы Фарадея
Таблица А.1 – Константы ионизации некоторых кислот и оснований
В присутствии аммиака ионы меди связываются, образуя внутреннюю сферу комплекса[Cu(NH3)4]2+:
Cu(OH)2 + 4NH3 [Cu(NH3)4]2+ + 2OH–
В соответствии с принципом Ле Шателье, чем больше концентрация аммиака, тем больше равновесие смещается вправо, тем больше растворимость гидроксида меди.
Рассмотренный пример интересен также тем, что реакцией обмена из слабого малорастворимого основания получается сильное растворимое основание (однако причина обмена – образование слабого электролита – комплексного соединения).
Пример 9. Как влияет pH на растворимость хромата свинца (II)?
Решение: напишем уравнение равновесия для насыщенного раствора PbCrO4: PbCrO4 Pb2+ + CrO42–.
а) увеличение кислотности раствора приведет к увеличению растворимости соли вследствие связывания хромат-ионов (см. пример7).
б) увеличение концентрации гидроксид-ионов может привести к образованию гидроксокомплекса (т. к. свинец – амфотерный металл):
PbCrO4 + 4OH– [Pb(OH)4]2– + CrO42–; таким образом, чем больше концентрация гидроксид-ионов (т. е. чем больше pH раствора), тем больше растворимость соли.
Из (а) и (б) следует, что минимальная растворимость PbCrO4 обеспечивается в растворах с реакцией среды, близкой к нейтральной.
Применение гетерогенных равновесий в качественном анализе. Разделение ионов методом дробного осаждения малорастворимых электролитов
Образование осадков (часто характерной окраски) является одним из вариантов качественного анализа растворов электролитов. При этом различие в растворимости солей и оснований используется и как основной метод открытия ионов, и как дополнительный, если смесь ионов требуется предварительно разделить.
Пример 10. Предложить способ разделения в водном растворе смеси ионов магния, алюминия и железа (III) при равных их концентрациях в растворе, С(Меn+) = 0,1 M.
Решение
Все три заданных металла образуют малорастворимые гидроксиды, причем один из них – гидроксид алюминия – амфотерный; следовательно, при избытке щелочи алюминий легко отделяется от магния и железа.
Для разделения магния и железа рассчитаем pH осаждения их гидроксидов:
– напишем выражение ПР для гидроксида магния:
ПР = [Mg2+][OH-]2 = 610–10;
– рассчитаем pH начала осаждения гидроксида при С(Mg2+) = 0,1 М:
С(OH
–) =
– напишем выражение ПР для гидроксида железа (III):
ПР = [Fe3+] [OH–]3 = 610–38;
– рассчитаем pH начала осаждения гидроксида при С(Fe3+) = 0,1 М:
С(OH–) =
Таким образом, ионы железа и магния легко разделяются при постепенном увеличении pH раствора.
Примеры расчетов, показанные выше, не следует абсолютизировать. Растворение – физико-химический процесс, энергетика которого довольно сложная. Так, например, обсуждая влияние природы вещества на его растворимость, необходимо помнить, что затраты энергиина разрушение связеймежду ионами в твердом веществе при переводе их в раствор зависят не только от химической природы электролита, но и от величины его кристаллов. Чем крупнее кристаллы, тем меньше энергия системы при равном количестве содержащегося в них вещества,тем меньше растворимость. Кроме того, реальные кристаллы всегда имеют дефекты, которые могут быть как механическими, так и физико-химическими (например, обусловленные встройкой в узлы ионной решетки примесных катионов или анионов). На растворимость ионных соединений существенно влияет ионная сила раствора и ряд других факторов, которые обычно рассматриваются в курсах физической, коллоидной и аналитической химии. В процессе изучения этих дисциплин знания, полученные в курсе общей химии, будут все более дополняться и совершенствоваться.
9 Комплексные соединения
Состав, строение и свойства соединений, которые позднее назвали комплексными (или координационными), в свое время не вписывались в сложившиеся представления химической теории. Так, некоторые вещества, способные к самостоятельному существованию, оказались способными соединяться друг с другом, хотя валентные возможности атомов, казалось, уже исчерпаны. Например, FeF3 и KF способны образовать соединение состава FeF3·3KF, а CuSO4 и NH3 – соединение CuSO4·4NH3
. Причем, если ионы Cu2+ и Fe3+ в растворах CuSO4 и FeF3, соответственно, легко обнаружить с помощью реакций обмена (например, действием щелочи), то в приведенных выше их «комплексах» наличие Cu2+ и Fe3 тем же способом не обнаруживается.
Были непонятными, с позиций обычных обменных реакций, некоторые ионно-молекулярные взаимодействия. Так, при добавлении концентрированной соляной кислоты к голубому раствору CuSO4 окраска его менялась на зеленую. Розовый раствор CoCl2 при его выпаривании становился синим без добавления каких-либо реактивов. Какие «слабые электролиты» при этом образовались? Более того, оказались возможными реакции, прямо противоположные «привычным» обменным взаимодействиям. Например, при смешивании Cu(OH)2 и аммиака, осадок не образовывался, а растворялся, и вместо двух слабых оснований получалась щелочь. И, наконец, были получены вещества одинакового состава, но разного строения – изомеры. Ранее свойство изомерии было известно только для органических соединений.
Систематизировать и осмыслить перечисленные выше свойства и явления в течение более чем 100 лет пытались многие ученые, но наиболее полно это удалось сделать швейцарскому химику А. Вернеру (за что впоследствии ему была присуждена Нобелевская премия).
Основные положения координационной теории
Согласно теории А. Вернера, отличительной особенностью координационных соединений является наличие центрального атома(иона) металла, который называют комплексообразователем. Типичные комплексообразователи – катионы металлов побочных подгрупп: Ag+, Cu2+, Fe3+ и др.
В ближайшем окружении центрального атома располагаются ковалентно с ним связанные анионы кислот или электронейтральные молекулы, которые называют лигандами. Типичные лиганды – анионы кислот (галогенид-ионы, CN-, NO2-), молекулы NH3, H2O и др.
Число связей, образуемых центральным атомом с лигандами, называют его координационным числом (КЧ), а число связей, образуемых каждым лигандом с центральным атомом называют дентатностьюлиганда.
Примеры монодентатных лигандов: Cl–, F–, Br–, I–, CN–, OH–, NH3, H2O.
К числу бидентатных лигандов относится H2N–CH2–CH2–NH2 – этилендиамин, оксалат-, карбонат-ионы и др.
Примером полидентатных лигандов может служить этилендиаминтетраацетат-ион (ЭДТА).
Примечание: КЧ центрального атома – сложная функция, зависящая от размера и заряда центрального атома и лигандов, но оно обычно в 2 раза больше заряда комплексообразователя; уточнить его, также как и наиболее характерные для него лиганды, можно с помощью справочника (см. далее – «константы нестойкости»).
Центральный атом с координированными вокруг него лигандами образуют внутреннюю сферукомплекса. При написании полной формулы комплекса внутреннюю сферу выделяют квадратными скобками.
Заряд внутренней сферы равен алгебраической сумме зарядов центрального атома и всех лигандов. Например: [FeF6]3-, [Ag(NH3)2]+, [Co(H2O)4Cl2].
Если заряд внутренней сферы не равен нулю, то имеется внешняя сфера, состоящая из ионов с противоположным знаком (эти ионы могут быть также комплексными). Последовательность записи формулы комплекса определяется зарядами внешней и внутренней сфер: сначала пишут катион, затем – анион. Например: K3[FeF6], [Ag(NH3)2]2(SO4), [Co(NH3)6][Cr(CN)6]. Внутренняя сфера комплекса может быть смешанной (включать не одинаковые, а разные лиганды): [Co(NH3)5Cl]SO4.

Изомерия комплексных соединений
Изомерия проявляется в существовании соединений с одинаковым составом, но различным строением, вследствие чего эти соединения обладают разными свойствами.
Цис- или транс- изомерия возможна для комплексов со смешанной внутренней сферой квадратного или октаэдрического строения и обусловлена различным пространственным расположением пары одинаковых лигандов относительно центрального атома. Если одинаковые лиганды располагаются в соседних вершинах квадрата или октаэдра, то такой изомер называется цис-изомером, если в противоположных – транс-изомером (рисунок 9.1).
Геометрические (или цис-, транс-) изомеры
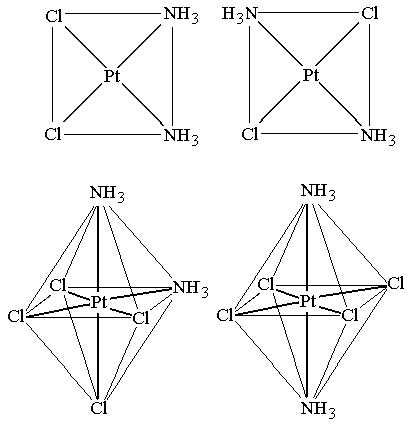
цис – транс –
Рисунок 9.1 – Цис-, транс - изомеры [Pt(NH3)2Cl2] и [Pt(NH3)2Cl4]
Гидратные изомеры различаются распределением молекул воды между внутренней и внешней сферами:
[Cr(H2O)6]Cl3 [Cr(H2O)5
Cl]Cl2H2O [Cr(H2O)4Cl2]Cl2H2O
Ионизационные изомеры различаются распределением лигандов-анионов между внутренней и внешней сферами:
[Co(NH3)4Br2]Cl и [Co(NH3)4BrCl]Br
[Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2
Координационная изомерия возможна для комплексных соединений, у которых и катион и анион комплексные, и обусловлена переходом лигандов от одного комплексообразователя к другому:
[Co(NH3)6][Cr(CN)6] [Cr(NH3)6][Co(CN)6]
Классификация комплексов
а) классификация по заряду внутренней сферы
Как отмечалось ранее, заряд внутренней сферы комплекса равен алгебраической сумме зарядов комплексообразователя и лигандов. Если этот заряд положительный, то комплекс относят к катионным, если отрицательный – к анионным, если нулевой – к неэлектролитам.
Примеры:
[Cu(H2O)4]SO4, [Ni(NH3)6]Cl2, [Pt(NH3)4Br2]Cl2 – катионные комплексы;
Na3[Al(OH)6], K3[FeF6], K[Co(NH3)2(CN)4] – анионные комплексы;
[Pt(NH3)2Cl4], [Ni(CO)4], [Cr(C6H6)2 – комплексные неэлектролиты.
б) классификация по типу лигандов
– аминокомплексы – комплексы, в которых функцию лигандов выполняют молекулы аммиака или другие амины: [Cu(NH3)4]SO4, [Pt(en)3]Cl4 (en – этилендиамин H2N(CH2)2NH2).
– аквакомплексы – комплексы, в которых функцию лигандов выполняют молекулы воды: [Cu(H2O)4]SO4, [Cr(H2O)6]Cl3, [Al(H2O)6]Cl3 .
– гидроксокомплексы – комплексы, в которых функцию лигандов выполняют гидроксид-ионы: K3[Cr(OH)6], Na2[Zn(OH)4] .
– ацидокомплексы – комплексы, в которых функцию лигандов выполняют анионы кислот: K2[PtCl6], K2[SiF6], K3[Fe(CN)6] .
Существуют также смешанные комплексы, в состав внутренней сферы которых входят различные типы лигандов.
Номенклатура комплексных соединений
Название комплексного соединения, как и название соли, начинают с названия аниона, за которым следует название катиона в родительном падеже. Для того чтобы освоить номенклатуру комплексных соединений, необходимо научиться правильно называть комплексные анионы и катионы.
Название комплексного иона (или электронейтральной комплексной частицы) начинают с указания числа лигандов и их типа. Число лигандов указывают греческими числительными: