Файл: Ббк 24. 2я7 с 23 Учебное пособие. Сборник тестовых заданий по биоорганической химии утверждено на заседании Ученого Совета Дон нму им. М. Горького.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 08.11.2023
Просмотров: 3471
Скачиваний: 37
СОДЕРЖАНИЕ
Краткий обзор строения и химических свойств углеводородов, спиртов, фенолов, тиолов и аминов
Строение и химические свойства альдегидов, кетонов
Строение и химические свойства моно- и дикарбоновых кислот
Строение и химические свойства липидов и фосфолипидов
Строение и химические свойства окси, оксокислот
Углеводы. Строение и химические свойства ди- и полисахаридов
"Биогенные элементы, биологическая роль, применение в медицине"
"Биогенные элементы, биологическая роль, применение в медицине"
"Тепловые эффекты химических реакций. Химическая термодинамика"
"Кинетика биохимических реакций. Химическое равновесие"
"Растворы. Способы выражения состава растворов"
"Растворы. Перманганатометрия как метод объемного анализа"
Кислотно-основное равновесие в организме. Водородный показатель"
"Буферные системы, классификация и механизм действия"
"Коллигативные свойства растворов. Осмос и осмотическое давление"
-
Крахмал -
Гепарин -
Хондроитинсульфат -
Целлюлоза -
Гиалуроновая кислота
332. Полисахариды соединительной ткани называют иногда кислыми мукополисахаридами, так как они содержат в своей структуре две группы, обусловливающие их анионное строение. Определите такие группы:
-
–ОН, –СОNH2 -
–NH2, –ОН -
–SH, –NO2 -
–SO3H, –СООН -
–CN
333. При помощи физико-химического анализа была установлена структура полисахарида:

Укажите название данного углевода:
-
Целлюлоза -
Амилоза -
Гликоген -
Гепарин -
Сахароза
АМИНОКИСЛОТЫ
334. В каждой макромолекуле белка α-аминокислоты, являющие его структурными компонентами, соединены между собой пептидной связью. Укажите данную группу атомов:
| 1. |  |
| 2. |  |
| 3. |  |
| 4. |  |
| 5. | 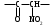 |
335. Аланин – одна из наиболее важных α-аминикислот, входящих в состав белков. Укажите, реакцию среды, которую имеет эта кислота в водном растворе:
 |
-
pH =5 -
pH = 7 -
pH = 9 -
pH = 11 -
pH = 3
336. Некоторые α–аминокислоты, необходимые для синтеза белков, не синтезируются в организме, а должны поступать извне. Укажите название таких аминокислот:
-
β -аминокислоты -
α -аминокислоты -
Протеиды -
Незаменимые -
γ-аминокислоты
337. В ходе лабораторной работы студенты изучали свойства аминокислот. Укажите, реакцией с какими веществами можно доказать их амфотерность:
-
NaOH и KCN -
HCl и C2H5OH -
NaOH и HCl -
C2H5OH и KOH -
HNO2 и NaCl
338. Аминокислоты являются универсальным биологическим материалом, благодаря способности полимеризоваться. Укажите связь, при помощи которой они соединяются в цепь:
-
Водородная -
Электростатическая -
Пептидная -
Гидрофобная -
Дисульфидная
339. Для аминокислот существует несколько видов классификаций, одна из которых учитывает количество амино- и карбоксильных групп в структуре молекулы. Классифицируйте приведенную аминокислоту в зависимости от данного признака:
 |
-
Моноаминомонокарбоновая -
Моноаминодикарбоновая -
Диаминомонокарбоновая -
Диаминодикарбоновая -
Моноаминотрикарбоновая
340. В лаборатории для обнаружения α-аминокислот использовали качественную реакцию. Укажите ее название:
-
Биуретовая реакция -
Нингидриновая -
Метод Ван-Слайка -
Формольное титрование -
Диспропорционирование
341. С целью идентификации аминокислот применили ксантопротеиновую реакцию. Укажите аминокислоту, которая при проведении реакции дает желтое окрашивание:
| 1. |  |
| 2. |  |
| 3. |  |
| 4. |  |
| 5. |  |
342. В организме аминокислоты подвергаются дезаминированию. Укажите, какое дезаминирование является преобладающим в тканях человека:
-
Восстановительное -
Окислительное -
Гидролитическое -
Неокислительное -
Внутримолекулярное
343. В процессе синтеза был получен дипептид:

Укажите его название:
-
Гли–Ала -
Ала–Ала -
Лиз–Ала -
Сер–Лиз -
Лиз–Гли
344. Произошло разрушение пространственной формы белка при сохранении его первичной структуры. Укажите название данного явления:
-
Денатурация -
Эпимеризация -
Деструкция -
Конденсация -
Полимеризация
345. Для аминокислот характерна стереоизомерия, поэтому для обозначения их конфигурации применяют D, L – систему. Укажите, конфигурацию аминокислот, входящих в состав белков человека:
-
β, D аминокислоты -
α, D аминокислоты -
α, L аминокислоты -
β, L аминокислоты -
γ, L аминокислоты
346. В зависимости от природы радикала аминокислоты (АК) относятся к различным группам. Укажите, к какой группе можно отнести фениаланин:

-
Гетероциклические -
Ароматические -
Алифатические -
-аминокислоты -
γ-аминокислоты
347. Аминокислоты существуют в растворе в разных ионных формах. Укажите фактор, от которого это зависит:
-
Природа растворителя -
Степень диссоциации -
рН раствора. -
Концентрация аминокислоты. -
Температура
348. Аминокислота глицин прореагировала с уксусным альдегидом. Укажите конечный продукт данной реакции:
-
Соль -
Лактон -
Кислота -
Имин -
Спирт
349. По кислотно-основным свойствам аминокислоты делятся на несколько групп. Укажите аминокислоту, относящуюся к основным:
| 1. |  |
| 2. |  |
| 3. |  |
| 4. |  |
| 5. |  |
350. Аминокислоты вступают в реакции со спиртами. Укажите класс соединений, образующийся при этом:
-
Спирты -
Имины -
Альдегиды -
Кислоты -
Сложные эфиры
351. Аминокислоты биологически активные соединения, для которых характерна стереоизомерия. Укажите количество ассиметрических атомов углерода в молекуле -аминопропионовой кислоты:
-
Один -
Два -
Три -
Четыре -
Пять
352. Аминокислота гистидин в своей структуре содержит гетероциклический радикал. Укажите гетероцикл, радикал которого входит в структуру данной аминокислоты:

-
Пиридин -
Индол -
Пиразол -
Пиримидин -
Имидазол
353. В организме человека глутаминовая кислота подвергается дезаминированию:

Укажите образующиеся при этом продукты:
-
α-Оксокислота и аммиак -
Альдегид и вода -
Кетон и аммиак -
β-Оксикислота и вода -
Молочная кислота и азот
354. Для идентификации определенных аминокислот применили реакцию с концентрированной нитратной кислотой, в результате которой наблюдали появление желтой окраски раствора. Укажите название данной реакции:
-
Нингидриновая -
Ксантопротеиновая -
Мурексидная -
Биуретовая -
Изонитрильная
355. Белки состоят из аминокислотных фрагментов и обладают различными уровнями структурной организации. Укажите определение, описывающее первичную структуру белка:
-
Полинуклеотидная цепь -
Полипептидная цепь -
Полисахаридная цепь -
Смесь аминокислот -
Полиамидная цепь
356. Аминокислоты могут взаимодействовать между собой и образовывать длинные пептидные цепи. Укажите функциональные группы, участвующие в этом процессе:
-
Гидроксильные а аминогруппы -
Гидроксильные группы -
Карбоксильные группы -
Аминогруппы и карбонильные -
Аминогруппы и карбоксильные
357. Ферменты являются полипептидными веществами. Укажите, при помощи какой реакции можно определить наличие пептидной связи в их составе:
-
Биуретовая реакция -
Ксантопротеиновая реакция -
Метод Ван-Слайка -
Реакция формольного титрования -
Реакция серебряного зеркала
358. L-Аспарагиновая кислота в организме под действием фермента аспартазы подвергается неокислительному дезаминированию. Укажите конечный продукт реакции дезаминирования данной кислоты: